
57£®(09Č«¹ś¢ń)ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ĘųĢå¶ŌĘ÷±ŚµÄŃ¹Ēæ¾ĶŹĒ“óĮæĘųĢå·Ö×Ó×÷ÓĆŌŚĘ÷±Śµ„Ī»Ć껿ÉĻµÄĘ½¾ł×÷ÓĆĮ¦
B£®ĘųĢå¶ŌĘ÷±ŚµÄŃ¹Ēæ¾ĶŹĒ“óĮæĘųĢå·Ö×Óµ„Ī»Ź±¼ä×÷ÓĆŌŚĘ÷±ŚÉĻµÄĘ½¾ł³åĮæ
C£®ĘųĢå·Ö×ÓČČŌĖ¶ÆµÄĘ½¾ł¶ÆÄܼõŠ”£¬ĘųĢåµÄŃ¹ĒæŅ»¶Ø¼õŠ”
D£®µ„Ī»Ģå»żµÄĘųĢå·Ö×ÓŹżŌö¼Ó£¬ĘųĢåµÄŃ¹ĒæŅ»¶ØŌö“ó
56£® (06±±¾©)ČēĶ¼ĖłŹ¾£¬Į½øöĻąĶصÄČŻĘ÷P”¢Q¼ä×°ÓŠ·§ĆÅK”¢PÖŠ³äĀśĘųĢ壬QĪŖÕęæÕ£¬ÕūøöĻµĶ³ÓėĶā½ēƻӊČČ½»»»£®“ņæŖ·§ĆÅKŗó£¬PÖŠµÄĘųĢå½ųČėQÖŠ£¬×īÖÕ“ļµ½Ę½ŗā£¬Ōņ
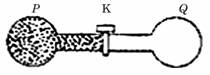
A£®ĘųĢåĢå»żÅņÕĶ£¬ÄŚÄÜŌö¼Ó””””””””””””””””””
B£®ĘųĢå·Ö×ÓŹĘÄܼõÉŁ£¬ÄŚÄÜŌö¼Ó C£®ĘųĢå·Ö×ÓŹĘÄÜŌö¼Ó£¬Ń¹ĒææÉÄܲ»±ä””””””””””
D£®QÖŠĘųĢå²»æÉÄÜ×Ō·¢µŲČ«²æĶĖ»Ųµ½PÖŠ
55£®(05Č«¹ś)ČēĶ¼ĖłŹ¾£¬¾ųČČøō°åK°Ń¾ųČȵÄĘųø×·Öøō³ÉĢå»żĻąµČµÄĮ½²æ·Ö£¬KÓėĘųø×±ŚµÄ½Ó“„ŹĒ¹ā»¬µÄ£®Į½²æ·ÖÖŠ·Ö±šŹ¢ÓŠĻąĶ¬ÖŹĮ攢ĻąĶ¬ĪĀ¶ČµÄĶ¬ÖÖĘųĢåaŗĶb£®ĘųĢå·Ö×ÓÖ®¼äĻą»„×÷ÓĆŹĘÄÜæÉŗöĀŌ£®ĻÖĶعżµēČČĖæ¶ŌĘųĢåa¼ÓČČŅ»¶ĪŹ±¼äŗó£¬a”¢bø÷×Ō“ļµ½ŠĀµÄĘ½ŗā
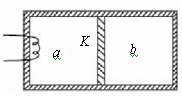
A£®aµÄĢå»żŌö“óĮĖ£¬Ń¹Ēæ±äŠ”ĮĖ””””””””””””””””””””””””
B£®bµÄĪĀ¶ČÉżøßĮĖ
C£®¼ÓČČŗóaµÄ·Ö×ÓČČŌĖ¶Æ±ČbµÄ·Ö×ÓČČŌĖ¶Æøü¼¤ĮŅ””””””
D£®aŌö¼ÓµÄÄŚÄÜ“óÓŚbŌö¼ÓµÄÄŚÄÜ
54£®(04¹ć¶«)ČēĶ¼ĖłŹ¾£¬ĆܱվųČČµÄ¾ßÓŠŅ»¶ØÖŹĮæµÄ»īČū£¬»īČūµÄÉĻ²æ·ā±Õ×ÅĘųĢ壬ĻĀ²æĪŖÕęæÕ£¬»īČūÓėĘ÷±ŚµÄĦ²ĮŗöĀŌ²»¼Ę£¬ÖĆÓŚÕęæÕÖŠµÄĒįµÆ»ÉµÄŅ»¶Ė¹Ģ¶ØÓŚČŻĘ÷µÄµ×²æ£®ĮķŅ»¶Ė¹Ģ¶ØŌŚ»īČūÉĻ£¬µÆ»É±»Ń¹ĖõŗóÓĆÉžŌś½ō£¬“ĖŹ±µÆ»ÉµÄµÆŠŌŹĘÄÜĪŖEP(µÆ»É“¦ÓŚ×ŌČ»³¤¶ČŹ±µÄµÆŠŌŹĘÄÜĪŖĮć)£¬ĻÖÉžĶ»Č»¶ĻæŖ£¬µÆ»ÉĶĘ¶Æ»īČūĻņÉĻŌĖ¶Æ£¬¾¹ż¶ą“ĪĶłø“ŌĖ¶Æŗó»īČū¾²Ö¹£¬ĘųĢå“ļµ½Ę½ŗāĢ¬£¬¾¹ż“Ė¹ż³Ģ

A£®EPČ«²æ×Ŗ»»ĪŖĘųĢåµÄÄŚÄÜ
B£®EPŅ»²æ·Ö×Ŗ»»³É»īČūµÄÖŲĮ¦ŹĘÄÜ£¬ĘäÓą²æ·ÖČŌĪŖµÆ»ÉµÄµÆŠŌŹĘÄÜ
C£®EPČ«²æ×Ŗ»»³É»īČūµÄÖŲĮ¦ŹĘÄÜŗĶĘųĢåµÄÄŚÄÜ
D£®EPŅ»²æ·Ö×Ŗ»»³É»īČūµÄÖŲĮ¦ŹĘÄÜ£¬Ņ»²æ·Ö×Ŗ»»ĪŖĘųĢåµÄÄŚÄÜ£¬ĘäÓą²æ·ÖČŌĪŖµÆ»ÉµÄµÆŠŌŹĘÄÜ
53£®(03Č«¹ś)ČēĶ¼ĖłŹ¾£¬¹Ģ¶ØČŻĘ÷¼°æɶƻīČūP¶¼ŹĒ¾ųČČµÄ£¬ÖŠ¼äÓŠŅ»µ¼ČČµÄ¹Ģ¶Øøō°åB£¬BµÄĮ½±ß·Ö±šŹ¢ÓŠĘųĢå¼×ŗĶŅŅ£®ĻÖ½«»īČūP»ŗĀżµŲĻņBŅʶÆŅ»¶Ī¾ąĄė£¬ŅŃÖŖĘųĢåµÄĪĀ¶ČĖęĘäÄŚÄܵÄŌö¼Ó¶ųÉżøߣ®ŌņŌŚŅʶÆPµÄ¹ż³ĢÖŠ
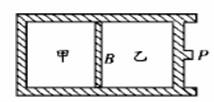
A£®ĶāĮ¦¶ŌŅŅ×ö¹¦£»¼×µÄÄŚÄܲ»±ä””””””
B£®ĶāĮ¦¶ŌŅŅ×ö¹¦£»ŅŅµÄÄŚÄܲ»±ä
C£®ŅŅ“«µŻČČĮæøų¼×£»ŅŅµÄÄŚÄÜŌö¼Ó””””
D£®ŅŅµÄÄŚÄÜŌö¼Ó£»¼×µÄÄŚÄܲ»±ä
52£®(06½ĖÕ)ÓĆøō°å½«Ņ»¾ųČČČŻĘ÷øō³ÉAŗĶBĮ½²æ·Ö£¬AÖŠŹ¢ÓŠŅ»¶ØÖŹĮæĄķĻėĘųĢ壬BĪŖÕęæÕ(Ķ¼¢Ł)”£ĻÖ°Ńøō°å³éČ„£¬AÖŠµÄĘųĢå×Ō¶Æ³äĀśÕūøöČŻĘ÷(Ķ¼¢Ś)£¬Õāøö¹ż³Ģ³ĘĪŖĘųĢå×ŌÓÉÅņÕĶ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
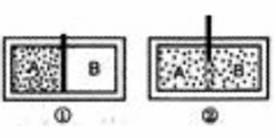
A£®×ŌÓÉÅņÕĶ¹ż³ĢÖŠ£¬ĘųĢå·Ö×ÓÖ»×÷¶ØĻņŌĖ¶Æ
B£®×ŌÓÉÅņÕĶĒ°ŗó£¬ĘųĢåµÄŃ¹Ēæ²»±ä ””””””””
C£®×ŌÓÉÅņÕĶĒ°ŗó£¬ĘųĢåµÄĪĀ¶Č²»±ä
D£®ČŻĘ÷ÖŠµÄĘųĢåŌŚ×ć¹»³¤µÄŹ±¼äÄŚ£¬ÄÜČ«²æ×Ō¶Æ»Ųµ½A²æ·Ö
29£®(16·Ö)ŅŃÖŖ£ŗ¢ŁŅ»¶ØĢõ¼žĻĀ£¬R-Cl + 2Na + Cl-R'”śR-R'+ 2NaCl
¢ŚČ©ŗĶ“¼æÉŅŌ·¢ÉśŃõ»Æ·“Ó¦£¬Ļą¹ŲĪļÖŹ±»Ńõ»ÆµÄÄŃŅדĪŠņŹĒ£ŗ””””””””””””””””””””
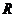
 ””””””””””””””””””””””””””””””””””””””””””””””””
””””””””””””””””””””””””””””””””””””””””””””””””
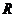
 RCHO×īŅ×£¬R-CH2OH“ĪÖ®£¬”” ””””CHOH×īÄŃ
RCHO×īŅ×£¬R-CH2OH“ĪÖ®£¬”” ””””CHOH×īÄŃ
”””” ĻÖӊijĀČ“śĢžA£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ78.5£»BÓėĀČĘų·“Ӧɜ³ÉµÄŅ»ĀČ“śĪļÓŠĮ½ÖÖ”£ÓŠ¹ŲµÄ×Ŗ»Æ¹ŲĻµČēĻĀĶ¼ĖłŹ¾(²æ·Ö²śĪļ¼°Ģõ¼ž¾łŅŃĀŌČ„)£»
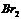
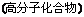
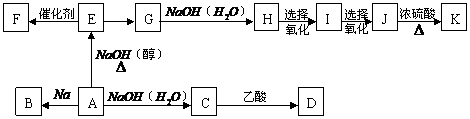
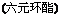
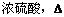
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)·“Ó¦ĄąŠĶ£ŗA”śE ”””””””””””””””””””””””””””” £¬E”śF”””””””””””””””” £»
(2)½į¹¹¼ņŹ½£ŗB”””””””””””””””””””””””””””””””””” £¬F”””””””””””””””””””””” £¬I”””””””””””””””””””””” £»
(3)·“Ó¦·½³ĢŹ½£ŗA”śE”””””””””””””””””””””””””””””””””””””””””””””””””””” £»
J”śK”””””””””””””””””””””””””””””””””””””””””””””””””””””””” £»
G”śH”””””””””””””””””””””””””””””””””””””””””””””””””””””” £»
(4)DµÄĶ¬·ÖŅģ¹¹ĢåÄÜ·¢ÉśÖŠŅų¾µ·“Ó¦£¬²»ÄÜ·¢ÉśĖ®½ā·“Ó¦£¬Ņ²²»ĻŌĖįŠŌµÄÓŠ¶ąÖÖ£¬ĒėŠ“³öČĪŅā2ÖÖ”””””””””””””””””””””””””” ”””””””””””””””””””” ”””””””””””””””””””” ”£
28£®(14·Ö)A”¢B”¢C”¢D”¢E”¢FŹĒ֊ѧ»Æѧ֊³£¼ūµÄ6ÖÖĪļÖŹ£¬ĖüĆĒŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌ·¢ÉśČēĻĀ·“Ó¦£ŗ
¢ŁA+B”śC+D”” ¢ŚB+E”śD+F”” ¢ŪC+E”śA+F
(1)ČōA”¢D”¢EĪŖĀ±ĖŲµÄµ„ÖŹ£¬·“Ó¦¢Ł¢Ś¢Ū¾łĪŖČÜŅŗÖŠ½ųŠŠµÄÖĆ»»·“Ó¦£¬ŌņA”¢D”¢EÓėĒāĘų»ÆŗĻÓÉÄѵ½Ņ×µÄĖ³ŠņĪŖ”” ”””””””””””””””””””” £¬AøśB·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ””””””””
”””””””””””””” ”””””””””””””””””””””””””” ”” ”£
(2)³£ĪĀĻĀ£¬ČōDŹĒŅŗĢ¬½šŹō£¬AŹĒŗģÉ«¹ĢĢåµ„ÖŹ£¬·“Ó¦¢Ł¢Ś¢ŪŅ²¶¼ŌŚĖ®ČÜŅŗÖŠ½ųŠŠ£¬EŹĒ¶ĢÖÜĘŚµÄµ„ÖŹ£¬ĒŅŌŖĖŲµŲæĒÖŠŗ¬Įæ×ī¶ą£¬ŌņEæÉÄÜŹĒ”””””””””””””””””””””””””””””””””” £¬AøśB·“Ó¦µÄĄė×Ó·½³ĢŹ½”””””””””””””””””””””””””””””””””””””””””””””””” ”£
(3)ČōA”¢D”¢EŹĒµ„ÖŹ£¬CŹĒÓŠ“ÅŠŌµÄ¹ĢĢ壬FŹĒĪŽÉ«”¢ĪŽĪ¶”¢ÓŠ¶¾µÄĘųĢ壬ŌņAŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ”””””””””””””””””””””” ”””””””””””””””””””” ”””””””””””””” ”£
AŗĶB·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ”””””””””””””””””””””””””””””””””” ””””””””””””””””””””””””””
BŗĶE·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ”””””””””””””””””””””””””””””””””””””””””” ”””””””””””””” ”£
27£®(14·Ö)A”¢B”¢CŗĶD“ś±ķŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒĀś×ćŅŌĻĀĢõ¼ž£ŗ¢ŁCµÄŌ×ÓŠņŹżŹĒA”¢BµÄŌ×ÓŠņŹżÖ®ŗĶ£¬A”¢C”¢DµÄ×īĶā²ćµē×Ó ŹżŗĶĪŖ13£»¢ŚDµÄŌ×ÓŠņŹżŹĒCµÄ2±¶£¬DµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļŹĒ¶žŌŖĒæĖį”£ĒėĢīæÕ£ŗ
(1)AŹĒ”””””””””””” ŌŖĖŲ£¬Dµ„ÖŹŠĪ³ÉµÄ¾§ĢåŹōÓŚ”””””””””””””””””” (Ģī¾§ĢåĄąŠĶ)£»


(2)Bµ„ÖŹµÄµē×ÓŹ½ĪŖ”””””””””””””””””””””””””” £¬»³öCŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼”””””””””””””” £»
(3)·Ö±šŠ“³öDµÄµ„ŗĖĄė×ÓÓėFe3+ŗĶAl3+·“Ó¦µÄĄė×Ó·½³ĢŹ½”””””””””””””””””””””””””””””” £»
(4)ŅŃÖŖ£ŗÓÉA”¢B”¢C”¢DĖÄÖÖŌŖĖŲ×é³ÉµÄĮ½ÖÖ»ÆŗĻĪļŌŚĖ®ČÜŅŗÖŠ·“Ó¦æÉÉś³ÉŅ»ÖÖĪŽÉ«ÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬ŌņÕāĮ½ÖÖ»ÆŗĻĪļ¶¼ŹĒÓÉ”””””””””””””””””” ¼ü¹¹³É£¬ŹŌŠ“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” ”””””” ”£
26£®(16·Ö)ŹŠŹŪŅŅČ©Ķس£ĪŖ40%×óÓŅµÄŅŅČ©ČÜŅŗ”£ŅŃÖŖŅŅČ©·Šµć20.80C¾ĆÖƵÄŅŅČ©ČÜŅŗ»į²śÉś·Ö²ćĻÖĻó£¬ÉĻ²ćĪŖĪŽÉ«ÓĶדŅŗĢ壬ĻĀ²ćĪŖĖ®ČÜŅŗ”£¾Ż²ā¶Ø£¬ÉĻ²ćĪļÖŹĪŖŅŅČ©µÄ¼ÓŗĻĪļ(C2H4O)n£¬ĖüµÄ·Šµć±ČĖ®µÄ·Šµćøߣ¬·Ö×ÓÖŠĪŽČ©»ł”£ŅŅČ©ŌŚČÜŅŗÖŠŅ×±»Ńõ»Æ”£ĪŖ“Ó±äÖŹµÄŅŅČ©ČÜŅŗÖŠĢįČ”ŅŅČ©(ČŌµĆµ½ČÜŅŗ)£¬æÉĄūÓĆČēĻĀ·“Ó¦ŌĄķ£ŗ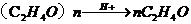 Ė¼æ¼ĻĀĮŠĪŹĢā²¢ĢīæÕ£ŗ
Ė¼æ¼ĻĀĮŠĪŹĢā²¢ĢīæÕ£ŗ


(1)ĻČ°Ń»ģŗĻĪļ·ÖĄėµĆµ½(C2H4O)n£¬½«»ģŗĻĪļ·ÅČė·ÖŅŗĀ©¶·£¬·Ö²ćĒåĪśŗó½ųŠŠ·ÖĄėµÄ²Ł×÷ŹĒ”””””””””””””””””””””””””””””””” ”£
(2)Ö¤Ć÷ŹĒ·ńŅŃÓŠ²æ·ÖŅŅČ©±»Ńõ»ÆµÄŹµŃé²Ł×÷ŗĶĻÖĻóŹĒ”””””””””””””””””””””””””””””””””””””””” ”£
(3)½«ÉŁĮæŅŅČ©ČÜŅŗµĪČėÅØĮņĖįÖŠ£¬Éś³ÉŗŚÉ«ĪļÖŹ”£
ĒėÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ÕāŅ»¹ż³Ģ””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””
(4)ĢįČ”ŅŅČ©µÄ×°ÖĆČēĶ¼ĖłŹ¾£ŗÉÕĘæÖŠ·ÅµÄŹĒ(C2H4O)nŗĶ6mol/LH2SO4µÄ»ģŗĻŅŗ£¬×¶ŠĪĘæÖŠ·ÅÕōĮóĖ®”£¼ÓČČÖĮ»ģŗĻŅŗ·ŠĢŚ£¬(C2H4O)n»ŗĀż·Ö½ā£¬Éś³ÉµÄĘųĢåµ¼ČĖ׶ŠĪĘæµÄĖ®ÖŠ”£
¢ŁÓĆĄäÄż¹ÜµÄÄæµÄŹĒ”””””””””””””””””””””””” ĄäÄżĖ®µÄ½ųæŚŹĒ(Ģī”°a”±»ņ”°b”±)”£”””””””””””””””””””””” £»
¢ŚÉÕĘæÖŠÓ¦»¹Šč¼Ó”””””””””””””””””””” ÄæµÄ”””””””””””””””””””””””””””””””””””””””””” ”£
¢ŪČōn=3£¬Ōņ(C2H4O)nµÄ½į¹¹¼ņŹ½ŹĒ”””””””””””””””””””””””””””””””””””””””””” ”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com