
30.第三代饮水净化工艺是以超滤膜为核心的直饮水生产工艺,能最有效地去除水中微生物。
纳滤膜是一种孔径约为1个纳米的过滤膜,1纳米(1nm)相当于( )
A.10-3米 B.10-6米 C.10-9米 D.10-12米
29.自来水深度处理工艺是在第一代工艺后增加臭氧、固体颗粒活性炭处理工序,这对控制有毒有害有机物比较有效。
(1)臭氧的化学式是____________;臭氧与氧气互为( )。
A.同系物 B.同素异形体 C.同位素 D.同分异构体
(2)在自来水生产过程中,疏松多孔的颗粒活性炭所体现的性质是( )。
A.氧化性 B.还原性 C.脱水性 D.吸附性
城市饮用水生产工艺经历了三个发展阶段。
28.第一代自来水生产工艺是“混凝-沉淀、过滤、消毒”净水工艺,流程如下:

(1)生产中用到净水剂,下列物质有净水作用的是( )(多选)。
A.石灰石 B.氧化铁 C.氯化铁 D.明矾
(2)上图生产流程中常用的消毒剂是氯气,常温下氯气为_________色气体,写出氯气溶于水与水反应的化学方程式__________________________________。潮湿的氯气有漂白性,真正起漂白作用的物质是____________(填写名称)。
(3)生产过程中两次加入消毒剂,其中“后加消毒剂”的目的是( )
A.使供水管网保持足够的余氯,防止水在管网中再次受到污染
B.氯气有毒,且很不稳定,一次加入会加大自来水的毒性
C.如果一次加入,氯气会堵塞管网,所以必须分两次加入
D.氯气难溶于水,一次加入时难全部溶解
(4)工业上一般性的过滤可以用丝网、布等,化学实验室里也常用过滤来分离某些混合物,化学实验室进行过滤操作时要用到的玻璃仪器有_________、____________、____________。
27.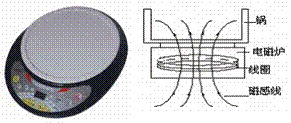 电磁炉原理图。炉内有一金属线圈,当电流通过线圈时产生磁场,该磁场又会引起电磁炉上面的铁质锅底内产生感应电流(即涡流),涡流使锅体铁分子高速无规则热运动,分子碰撞摩擦而产生热能,从而使锅体与食物温度迅速升高。故电磁炉煮食的热源来自于锅具本身而不是电磁炉本身发热传导给锅具,它是区别于靠热传导或微波来加热食物的新厨具。
电磁炉原理图。炉内有一金属线圈,当电流通过线圈时产生磁场,该磁场又会引起电磁炉上面的铁质锅底内产生感应电流(即涡流),涡流使锅体铁分子高速无规则热运动,分子碰撞摩擦而产生热能,从而使锅体与食物温度迅速升高。故电磁炉煮食的热源来自于锅具本身而不是电磁炉本身发热传导给锅具,它是区别于靠热传导或微波来加热食物的新厨具。
(1)完成下表:
|
项目 |
发热部位 |
对锅碗具的材质要求 |
|
微波炉 |
|
非金属材料 |
|
电磁炉 |
金属锅体 |
|
(2)假如想在网上查阅相关资料,写出一个你最关心的电磁炉问题: 。
26.LED可以直接把电转化为光。其优点是:①耗电低:LED工作电压2-3.6V,工作电流是0.02-0.03A;②寿命长:可达10万小时;③多变幻:可利用红绿蓝三基色原理,在计算机控制下使三种颜色具有256级灰度并任意混合,即可产生256×256×256=16777216种颜色,组合变化多端,实现丰富多彩的动态变化效果及图像。下表为常见发光体的大致效率(流明/瓦)(流明--光通量单位,数值大则单位时间内发光量大)。
|
白炽灯 |
日光灯 |
节能灯 |
钠灯 |
LED |
|
15 |
50 |
60-80 |
120 |
80-200 |
(1)用LED来制作手电,单支LED的用电功率最小的是 W;
(2)全彩大屏幕使用更随意,即使每天用10小时,它也可安全使用约 年(填整数)。
(3)若制作大屏幕的LED每种颜色都调在最大值,则显示为最亮的白色。若要显示出最黑色,请在下图右表的空白框内填上适当的值。
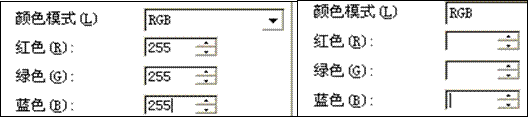
(4)节能灯正在取代白炽灯,其原因是 。
25.电梯工作原理如图。曳引绳两端分别连着轿厢和配重,靠曳引
绳与曳引轮摩擦产生的牵引力实现轿厢和配重的升降运动。固定在
轿厢上的导靴可沿着井道上的固定导轨往复升降运动防止轿厢在运
行中偏斜或摆动。设轿厢重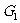 和配重
和配重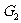 ,乘客总重
,乘客总重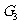 。
。
(1)配重的选择最好是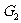 =
。
=
。
(2)若配重为6000N,某次运行时,轿厢下降的高度为4m,则配重
的重力势能增加了 J;
(3)在客流量比较大的公共场所,常常将两部电梯共用一部电机,并使
它们的轿厢与乘客互为配重。这样做的优点或缺点是 (可选)。
30.(15分)某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为(其中I、II为未知部分的结构):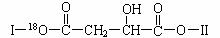 。为推测X的分子结构,现进行如下转化:
。为推测X的分子结构,现进行如下转化:
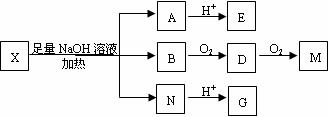
已知:E分子中检测到18O原子,向E的水溶液中滴入FeCl3溶液显紫色反应,且其苯环上的一氯代物只有一种;M的分子式为C2H2O4,M、G都能与NaHCO3溶液反应。又知芳香卤代烃的水解极其困难,即使在热的NaOH溶液中也不能发生水解。请回答下列问题:
(1)E分子中在同一直线上的原子最多有_____个。
(2)M的结构简式为______________。
(3)X的结构简式为__________________________。
(4)D溶液中加入新制Cu(OH)2悬浊液加热也可得到M,写出反应的化学方程式__________________。
(5)G可以转化为C4H4O4,该反应的有机反应类型为____________。
(6)写出两种与D的相对分子质量相同的有机物的分子式:①________;②_________。
29.(15分)在某反应体系中存在六种物质:Cr3+、S2O82-、Cr2O72-、H+、H2O和SO42-。已知在该反应中氧化反应只有Cr3+→Cr2O72-,反应过程中需要Ag+作催化剂,并加热。请回答下列问题:
(1)已知S2O82-离子中存在一个过氧键(-O-O-),则S2O82-离子中硫元素的化合价为__________价。
(2)写出该反应体系中发生反应的离子方程式:_______________________________。
(3)催化剂往往参加反应,改变反应途径。用两个离子方程式表示Ag+的催化过程:____________________________;________________________。
(4)若将上述反应设计成一个原电池,用石墨作电极,则其负极反应式为:_____________________,正极反应式为:____________________________。
28.(15分)已知某温度下,KW=1×10-13。A为酸溶液,其pH=a;B为碱溶液,其pH=b。
(1)若A为强酸,B为强碱,且a+b=13,两者等体积混合后,溶液的pH=________;若此时溶液中碱的阳离子浓度大于酸根阴离子浓度,其原因可能是(用文字表述)_____________________。
(2)若A为强酸,B为强碱,二者按体积比为1:10混合后溶液显中性,则a+b=____。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=13,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式 为_________________________________。
(4)在(3)的混合溶液中,微粒浓度大小关系一定正确的是___________(填序号)。
①c(MOH)>c(M+)>C(R-)>c(H+)>c(OH-)
②c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
③c(R-)>c(M+)>c(H+)>c(OH-)
④c(M+)>c(R-)>c(OH-)>c(H+)
⑤c(M+)+ c(H+)=c(R-)+c(OH-)
⑥c(MOH)=c(H+)-c(OH-)
27.(15分)某同学用如图一所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象。经过思考分析,该同学改用图二的装置,将气体收集在注射器中,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,结果都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生的现象明显比通入CO2快。
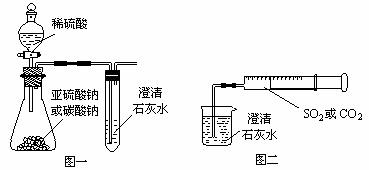
(1)若锥形瓶内装的是亚硫酸钠,写出锥形瓶内反应的化学方程式:______________
______________________________。
(2)对比分析两组实验,你认为用图一装置实验时,通入SO2不能出现浑浊的原因可能是____________________________________。写出此时试管内发生反应的总化学方程式:____________________________________。
(3)用图二装置实验时,以相同速率通入CO2或SO2,SO2产生浑浊再变澄清的现象比CO2快,其原因是___________________________________________。
(4)用图一进行SO2与石灰水反应的实验时,为防止SO2污染空气,应用盛有过量浓烧碱溶液的容器吸收SO2,写出容器内发生反应的离子方程式:____________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com