
15.化学实验中,常将溶液或试剂酸化,下列酸化处理的措施中正确的是
A.定性检验SO32-,将BaCl2溶液用HNO3酸化
B.为了提高KMnO4溶液的氧化能力,用盐酸将其酸化
C.检验某溶液中是否含Cl
– ,用HNO3酸化的AgNO3溶液
D.配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度
14. 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
3Zn + 2K2FeO4
+ 8H2O
3Zn(OH)2 +
2Fe(OH)3 + 4KOH
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
3Zn + 2K2FeO4
+ 8H2O
3Zn(OH)2 +
2Fe(OH)3 + 4KOH
下列叙述不正确的是
A.放电时负极反应为:Zn-2e-
+2OH-= Zn(OH)2
B.充电时阳极反应为:Fe(OH)3 -3e- + 5 OH- = FeO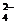 + 4H2O
+ 4H2O
C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
13.对胶体的下列叙述不正确的是
A.加电解质可使某种胶体聚沉,这是中和胶体粒子所带电荷的缘故
B.胶体粒子在直流电场中做定向移动,这是胶体粒子选择性吸附离子而带电荷的缘故
C.一束光线通过胶体时有丁达尔效应,这是胶体粒子对光散射的缘故
D.将溶质为1 mol的FeCl3饱和溶液滴入沸水中,制得的分散系中含Fe(OH)3胶体粒子数为NA
12.共价键、离子键和范德瓦耳斯力是粒子之间的三种作用力。下列晶体①Na2O2 ②SiO2 ③石墨 ④金刚石 ⑤NaCl ⑥白磷中,含有两种作用力的是
A.①②③ B.①③⑥ C.②④⑥ D.①②③⑥
11.碘的熔沸点低,其原因是
A.碘的非金属性较弱
B.I-I键的键能较小
C.碘晶体属于分子晶体
D.I-I共价键的键长较长
10.下列说法正确的是
A.需要加热的化学反应都是吸热反应 B.中和反应都是放热反应
C.原电池是将电能转化为化学能的一种装置
D水力发电是将化学能转化为电能的过程
9.右表为元素周期表中短周期的一部分。下列有关A、B、C、D、E五种元素的叙述中,不正确的是
A.A与B形成的阴离子可能有:AB32-、A2B42-
B.C的氢化物的沸点比E的氢化物的沸点高
C.D在过量的B中燃烧的主要产物为DB3
D.由这5种元素中的几种形成只含极性键的非极性分子不少于4种
8.下列说法不正确的是 ( )
A.硫酸厂生产过程中的污水,含有硫酸等杂质,可用石灰乳中和处理
B.充分利用硫酸厂生产过程中产生的
“废热”,可使硫酸厂向外界输出大量的能量
C.硫酸厂靠近原料产地比靠近硫酸消费中心更为有利
D.硫酸厂不应建在人口稠密的居民区和环保要求高的地区
|
|
||||
|
A |
|
B |
C |
|
|
|
|
D |
E |
|
7、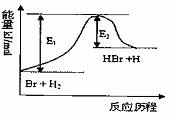 参照反应Br+H2
参照反应Br+H2 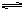 HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
A.
该反应的△H=+(E1-E2)kJ/mol
B. 加入催化剂,该化学反应的反应热变大
c.
升高温度可增大正反应速率,降低逆反应速率
D. 反应物总能量高于生成物总能量
6.
 2008年9月我国“神七”发射升空,中国航天员实现首次太空行走。运载火箭的原料用肼(N2H4)作为发动机的燃料,NO2为氧化剂,反应生成氮气和水蒸气。已知:
2008年9月我国“神七”发射升空,中国航天员实现首次太空行走。运载火箭的原料用肼(N2H4)作为发动机的燃料,NO2为氧化剂,反应生成氮气和水蒸气。已知:


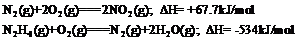


 下列判断正确的是( )
下列判断正确的是( )

 A.所有物质与氧气发生的化学反应都是放热反应
A.所有物质与氧气发生的化学反应都是放热反应

 B.
B.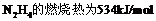


 C肼与
C肼与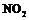 反应的热化学方程
反应的热化学方程 


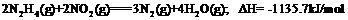


 D.3.2g肼完全反应转移的电子数为0.6mol
D.3.2g肼完全反应转移的电子数为0.6mol 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com