
13.(7分)此题为开放性题,答案比较多。
例如:生成沉淀的质量是多少克?或所取氯化钡固体的质量是多少克?等合理的补充。答案略。
(09达州)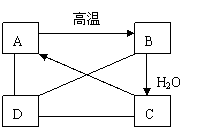 14.(6分)有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转
14.(6分)有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转
化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A。D与A、B、C均能
发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶
液反应,可产生不溶于稀硝酸的白色沉淀。
⑴请根据已知条件推断四种物质的化学式:
A B C D
⑵请写出下列反应的化学方程式:
C溶液中通入CO2,溶液变浑浊
D与A反应
13.(09达州)(7分)请根据下列已知条件设问,使其成为一道完整的计算题,然后解答。
一定质量的氯化钡(BaCl2)固体和100g溶质质量为9.8%的稀硫酸恰好完全反应。
28.(6分)
(1)无(1分)2.9%(2分)蒸发结晶(或蒸发)(1分)
(2)洗净并擦干(全写得1分,不全不给分)
(3)测温度变化(或用pH计测试或测反应前后溶液导电性)(1分)
28.(09苏州)(6分)酸与碱之间发生中和反应,其实质是酸溶液中大量自由移动的H+和碱溶液中大量自由移动的OH-结合成水分子的过程。请根据以下氢氧化钠溶液与稀盐酸反应的实验,回答问题。
[实验1]用酚酞试液
(1)向一锥形瓶中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为 ▲
色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为 ▲ (结果精确到0.1%)。反应后溶液中的溶质可用 ▲ 的方法(填一操作名称)使其析出。用酚酞作指示剂可逐滴控制酸、碱溶液反应的量,视觉效果灵敏,操作简便。
[实验2]用pH试纸
(2)向一支试管内倒入约2mL氢氧化钠溶液,再逐滴滴入盐酸,边滴边振荡。然后用玻璃棒蘸取反应液沾到pH试纸上,与标准比色卡对照。因无法通过肉眼观察到反应进程,需间隔数滴多次检测溶液的pH,所以每使用玻璃棒蘸取溶液前,必须进行 ▲ 的预处理。
[小 结]
(3)除了用酸碱指示剂、pH试纸外,还可用 ▲ (填力法)检测中和反应是否发生。
31.(09烟台)(6分)小青在实验室发现一瓶长期敞口放置的浓盐酸,为方便以后使用,他对其浓度进行了测定。取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)测定溶液的pH,得到的数据如下:
|
加入氢氧化钠的体积/mL |
0 |
1.0 |
8.0 |
9.5 |
10.5 |
12.0 |
16.5 |
|
烧杯中溶液的pH |
1.0 |
1.3 |
2.0 |
3.9 |
9.9 |
11.9 |
12.8 |
(1)请你绘制出烧杯中溶液的pH与加人氢氧化钠溶液体积(V)之间的变化关系图。
(2)请根据上图找出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积数,并据此计算此瓶盐酸的溶质质量分数。(氢氧化钠溶液的密度按1.0g/mL计算)
(1)(2分)评分要点:描点正确,曲线平滑。
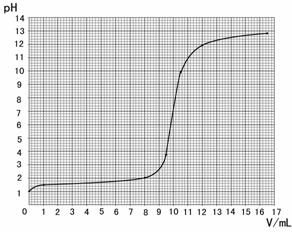
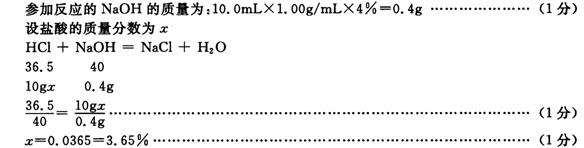 (2)解:由上图可知,恰好完全反应时消耗氢氧化钠溶液的体积约为10.0mL(9.7mL-10.3mL之间取值均可)……………………………………………………………………(1分)
(2)解:由上图可知,恰好完全反应时消耗氢氧化钠溶液的体积约为10.0mL(9.7mL-10.3mL之间取值均可)……………………………………………………………………(1分)
答:此瓶盐酸的溶质质量分数是3.65%。
31.(09嘉兴)在制取氢气实验时,同学们发现老师在准备用于反应的锌粒中滴人了少量的硫酸铜溶液。他们想:锌会与硫酸铜溶液反应生成铜,难道铜会影响锌和稀硫酸反应的快慢吗?他们决定对此开展有关实验:
(1)在设置对照组的时候,除了要控制好锌粒和稀硫酸的量之外,其中一组中要添加 ▲ 。
(2)实验中要比较锌和稀硫酸反应快慢,可以观察记录 ▲ 。
9.(09嘉兴)右图是某同学测量几种食品的pH后绘制的图象,其中偏碱性的是
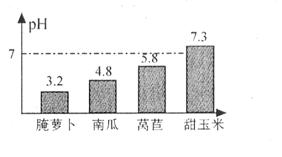 A.腌萝卜 B.南瓜
A.腌萝卜 B.南瓜
C.莴苣 D.甜玉米
26.(09杭州) (4分)实验室有两瓶标签脱落的溶液,只知道是盐酸溶液和硫酸溶液。请选择下列试剂:
①氧化铁②氢氧化钠溶液③碳酸钠溶液④氢氧化钡溶液⑤氯化钡溶液,用两种方法,每次只用一种试剂把它们鉴别出来。请填写下表:
|
|
选择的试剂编号 |
有明显反应现象的化学方程式 |
|
方法一 |
|
|
|
方法二 |
|
|
(09湖州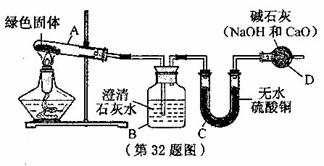 32 .绝大多数古代青铜器和铜器上都有绿色斑点,这些绿色斑点是铜长时间和氧气等物质发生化学反应生成的铜绿[ Cu2 ( OH )2 CO3 ] ,铜绿不稳定,受热后可分解生成三种物质。
32 .绝大多数古代青铜器和铜器上都有绿色斑点,这些绿色斑点是铜长时间和氧气等物质发生化学反应生成的铜绿[ Cu2 ( OH )2 CO3 ] ,铜绿不稳定,受热后可分解生成三种物质。
为探究铜绿受热后生成的物质,小莉同学从某种铜器上取下适量的铜绿,进行实验。 ① 连接装置如图,并检查装置的气密性。
② 将干燥后的铜绿放入试管A 中加热。
( l )试管口为什么要略向下倾斜?
( 2 ) A 装置中绿色固体逐渐变成黑色。取少量黑色固体放人另一试管中,加入稀硫酸,观察到黑色固体逐渐溶解,变成蓝色溶液。则可推测铜绿分解产物中有
( 3 ) B装置中澄清石灰水变浑浊,则可推测铜绿分解产物中 ( 4 ) C 装置中无水硫酸铜变蓝色,小莉同学认为铜绿分解产物中有水,但小明同学认为这还不能作出确切的推断。若要推断铜绿产物中是否有水,应如何改进实验装置?
59.SO3+2NaOH =Na2SO4+H2O(2分) 60 红 61 中和
62 都能使指示剂变色
63都能和某些非金属氧化物反应(或都能跟酸反应,其他合理答案均记分)
29.(09娄底)小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
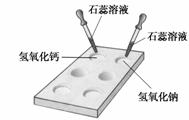 (1) 如右图所示,在白色点滴板上进行实验,请将实验现象填入下表:
(1) 如右图所示,在白色点滴板上进行实验,请将实验现象填入下表:
|
|
氢氧化钠溶液 |
氢氧化钙溶液 |
|
加紫色石蕊溶液 |
56 |
57 |
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方 程式 58 。
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式
 59 。
59 。
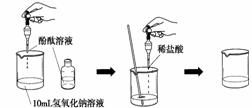
(4)如右图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显 60 色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。这一实验说明:酸与碱作用生成了盐和水,这一反应叫做 61 反应。
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质。(任写两点)
① 62
② 63
29题. 56. 溶液变蓝 57. 溶液变蓝 58.CO2+Ca(OH)2 =CaCO3↓+H2O(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com