

 2H2O+O2↑;双氧水在常温下就能分解,所以在反应前加入稳定剂的作用是防止双氧水分解.
2H2O+O2↑;双氧水在常温下就能分解,所以在反应前加入稳定剂的作用是防止双氧水分解. 2H2O+O2↑;防止双氧水分解.(2)C.
2H2O+O2↑;防止双氧水分解.(2)C. =
=
 =500g
=500g  ×100%=10.6%,y=447g
×100%=10.6%,y=447g -53g=447g
-53g=447g 

科目:初中化学 来源: 题型:阅读理解
 30、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.小健同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.
30、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.小健同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.| 序号 | 主要操作步骤 | 主要实验现象 | 操作目的 | |
| ① | 在集气瓶中加入少量 MnO2 (黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和水溶液;在分液漏斗b中加入稀盐酸 . |
|||
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 然后 用带火星的木条接近导管口 . |
带火星的木条复燃 . |
验证生成气体的成分 | ||
| 第②步操作得到的结论: “污渍爆炸盐”溶于水生成过氧化氢 . | ||||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 将生成的气体通入 澄清石灰水 . |
澄清石灰水变浑浊 . |
验证生成气体的成分 | ||
| 第③步操作得到的结论: “污渍爆炸盐”溶于水生成碳酸钠(或碳酸盐) . | ||||
查看答案和解析>>
科目:初中化学 来源: 题型:
 28、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种
28、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
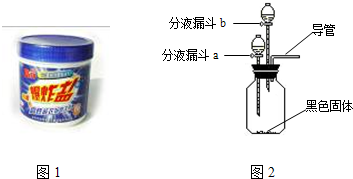
| 序号 | 主要操作步骤 | 主要实验现象 | 化学反应方程式 | |
| ① | 在集气瓶中加入少量 |
|||
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 然后 |
||||
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢 | ||||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 将生成的气体通入 |
验证生成气体的成分. | |||
| 第③步操作得到的结论:“污渍爆炸盐”溶于水生成碳酸钠 | ||||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
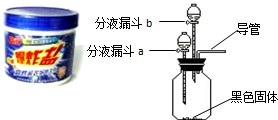 去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:| 序号 | 主要操作步骤 | 主要实验现象 | 操作目的 |
| ① | 在广口瓶中加入少量 二氧化锰 二氧化锰 (黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和水溶液;在分液漏斗b中加入稀盐酸 稀盐酸 . |
无 无 |
检验溶液中是否含有过氧化氢 检验溶液中是否含有过氧化氢 |
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验过氧化氢分解 检验过氧化氢分解 |
| 然后 用带火星的木条接近导管口 用带火星的木条接近导管口 . |
带火星的木条复燃 带火星的木条复燃 |
验证生成气体的成分 | |
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢. | |||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验碳酸钠和盐酸反应 检验碳酸钠和盐酸反应 |
| 将生成的气体通入 澄清石灰水 澄清石灰水 . |
澄清石灰水变浑浊 澄清石灰水变浑浊 . |
验证生成气体的成分 | |
| 第③步操作得到的结论:“污渍爆炸盐”溶于水生成碳酸钠. | |||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验装置 | 实验主要过程 |
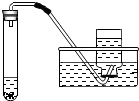 |
(1)检验装置气密性.操作如下:先将导管伸入液面下,用手紧握试管,观察到 导管口有气泡冒出 导管口有气泡冒出 ,松开手后,导管口有液面上升、(2)在试管中依次加入二氧化锰、过碳酸钠和水,有大量气泡生成 (3)收集满一瓶气体. (4)检验气体.方法是 将带火星的木条伸入集气瓶里,若带火星的木条复燃,则证明是氧气 将带火星的木条伸入集气瓶里,若带火星的木条复燃,则证明是氧气 . |
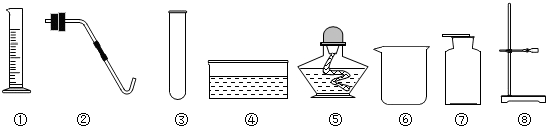
| 二氧化锰 |
| 二氧化锰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com