
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:阅读理解
 小娜同学发现厨房中有两瓶无标签的白色粉末,妈妈告诉她是苏打和小苏打.为了鉴别这两瓶白色粉末,小娜各取了一小包并将它们编号为A、B,然后进行实验探究.
小娜同学发现厨房中有两瓶无标签的白色粉末,妈妈告诉她是苏打和小苏打.为了鉴别这两瓶白色粉末,小娜各取了一小包并将它们编号为A、B,然后进行实验探究.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
复分解反应是我们学过的化学基本反应类型之一。学习时,应注意将知识进行归纳、总结,深刻理解复分解反应发生的条件,形成完整的知识体系。
( l )写出下列反应的化学方程式。
① 氯化钡溶液与硫酸钠溶液混合:______________________________;
② 碳酸钠溶液与稀盐酸混合:_______________________________;
③ 氢氧化钡溶液与稀硝酸混合:______________________________。
( 2 )你想过上述复分解反应为什么能够发生吗?
这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合。如上述反应①中,实际参加反应的离子是![]() 和
和![]() ,而
,而![]() 、
、![]() 则是“旁观者”,并没有参加反应。请你分析上述反应② 中实际参加反应的离子是_____;上述反应③ 中实际参加反应的离子是__________。
则是“旁观者”,并没有参加反应。请你分析上述反应② 中实际参加反应的离子是_____;上述反应③ 中实际参加反应的离子是__________。
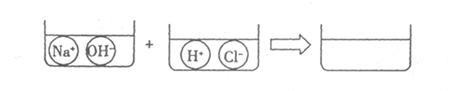
( 3 )请根据你的想象,在下图右边的容器中画出体现NaOH溶液和稀盐酸反应产物的示意图。
查看答案和解析>>
科目:初中化学 来源:2012年中考化学模拟试卷(6月)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com