
|
![]()
|
|
|
|
|
|

【提出问题】硬质玻璃管中的Ca是否完全转化为CaH2?
【查阅资料】
① 金属钙活动性很强,遇水反应生成氢氧化钙,同时产生一种气体;
② 氢化钙要密封保存,遇水反应放出氢气。
【猜想与实验】
1、 固体为Ca和CaH2。
2、 固体为CaH2。
甲同学的探究活动如下:
| 实验操作 | 实验现象 | 实验结论及解释 |
| ① 取少量硬质玻璃管中的固体于试管中,滴入少量的水,收集产生的气体,并用燃着的木条点燃 |
| 有氢气生成 |
| ② 继续向溶液中滴加酚酞 | 呈红色 | 生成 (填化学式) |
甲同学的结论:猜想1正确,固体为Ca和CaH2。
【实验反思】
乙同学认为由以上探究活动还不能得出猜想1正确,理由是 。请你帮助乙设计实验,写出主要的实验步骤、现象和相应的结论:
。
【反思讨论】
(1)写出CaH2与水反应的化学方程式 。
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是 。
(3)制备CaH2装置中,玻璃管a的作用是 。
甲同学的探究活动如下:
| 实验现象 | 实验结论及解释 |
| 冒气泡;气体燃烧,产生淡蓝色火焰 | |
| Ca(OH)2 |
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
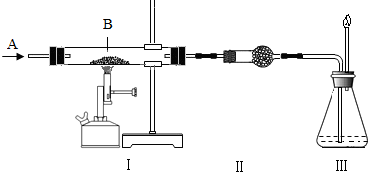
| 实验内容 | 实验现象 | 测量结果 |
| (1)使A持续通过装置Ⅰ、Ⅱ、Ⅲ | Ⅰ中B全变为黑色 | 黑色粉末为1.12克 |
| (2)当A与B在加热反应时 | Ⅱ中干燥管里的无水硫酸铜无变化 | |
| (3)实验结束 | Ⅲ中石灰水变浑浊 | Ⅲ中有1克沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数.取一定质量的赤铁矿粉与过量的木炭粉混合后,用如
化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数.取一定质量的赤铁矿粉与过量的木炭粉混合后,用如查看答案和解析>>
科目:初中化学 来源: 题型:
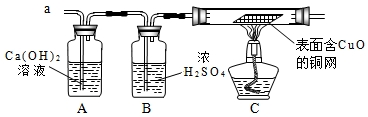
 某小组将一定质量的氧化铜粉末放入如图的装置中进行实验.分析该装置存在的问题后,你认为完善装置的具体方法是
某小组将一定质量的氧化铜粉末放入如图的装置中进行实验.分析该装置存在的问题后,你认为完善装置的具体方法是查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com