
(9分)铝、铁、铜是我们生活中常见的金属。
(1)铝制品具有很好的耐腐蚀性能,原因是 。
(2)铁生锈的条件是 ,生活中防止铁生锈的方法有
(写一种即可)。
(3)高炉中以赤铁矿(主要成分氧化铁)为原料炼铁的原理是 (用化学方程式表示)。
(4)为探究铝、铁、铜三种金属的活动性顺序,甲、乙、丙三位同学设计了如下实验方案(金属片已打磨),如图所示: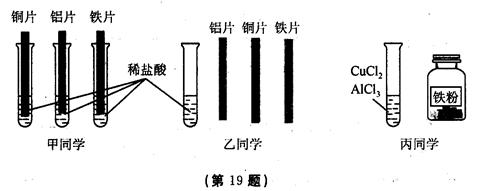
①甲同学根据铜片表面无变化的现象,判断出三种金属的活动性顺序为Al>Fe>Cu。
②乙同学只用一支试管,取一次稀盐酸也能证明Al>Fe>Cu。他在稀盐酸中插入金属的顺序为: 或 ,写出其中一个反应的化学方程式 。
③丙同学把一定量的铁粉放入CuCl2和AlCl3的混合溶液中,充分反应后过滤,向滤出的固体中加入稀盐酸,无明显现象,则滤液中一定含有的溶质是 。
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:初中化学 来源: 题型:
(9分)金属及材料在生活、生产中应用十分广泛。
1.铝、铁、铜是人类广泛使用的三种金属,人类开始使用这三种金属的先后排序为___(用元素符号表示);
2.目前人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁的硬度 (填“大”或“小”);
3.铝制器皿在空气中形成具有保护作用的薄膜,它的成分是 ,铁制品表面易生锈,用盐酸除去铁锈的反应方程式为 ,该反应的基本类型是 。
4.将mg氧化铜加入稀硫酸中完全溶解后,再加入铁粉充分反应,过滤,得到滤渣A和滤液B。再将滤渣A加入足量稀硫酸中,有气泡冒出,充分反应后,剩余固体物质的质量为3.2g。则滤渣A的成分是__________,原氧化铜的质量m=______________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2012年广东省广州市萝岗区中考一模化学试卷 (带解析) 题型:填空题
(9分)金属及材料在生活、生产中应用十分广泛。
【小题1】铝、铁、铜是人类广泛使用的三种金属,人类开始使用这三种金属的先后排序为___(用元素符号表示);
【小题2】目前人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁的硬度 (填“大”或“小”);
【小题3】铝制器皿在空气中形成具有保护作用的薄膜,它的成分是 ,铁制品表面易生锈,用盐酸除去铁锈的反应方程式为 ,该反应的基本类型是 。
【小题4】将mg氧化铜加入稀硫酸中完全溶解后,再加入铁粉充分反应,过滤,得到滤渣A和滤液B。再将滤渣A加入足量稀硫酸中,有气泡冒出,充分反应后,剩余固体物质的质量为3.2g。则滤渣A的成分是__________,原氧化铜的质量m=______________g。
查看答案和解析>>
科目:初中化学 来源:2012年初中毕业升学考试(辽宁锦州卷)化学(解析版) 题型:简答题
(9分)铝、铁、铜是我们生活中常见的金属。
(1)铝制品具有很好的耐腐蚀性能,原因是 。
(2)铁生锈的条件是 ,生活中防止铁生锈的方法有
(写一种即可)。
(3)高炉中以赤铁矿(主要成分氧化铁)为原料炼铁的原理是 (用化学方程式表示)。
(4)为探究铝、铁、铜三种金属的活动性顺序,甲、乙、丙三位同学设计了如下实验方案(金属片已打磨),如图所示:
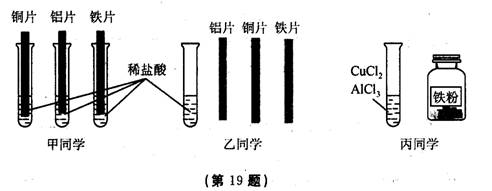
①甲同学根据铜片表面无变化的现象,判断出三种金属的活动性顺序为Al>Fe>Cu。
②乙同学只用一支试管,取一次稀盐酸也能证明Al>Fe>Cu。他在稀盐酸中插入金属的顺序为: 或 ,写出其中一个反应的化学方程式 。
③丙同学把一定量的铁粉放入CuCl2和AlCl3的混合溶液中,充分反应后过滤,向滤出的固体中加入稀盐酸,无明显现象,则滤液中一定含有的溶质是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com