
现有13.7 g由Na2CO3与NaHCO3组成的混合物,其中Na2CO3占5.3 g,请计算
(1)混合物中碳元素与氧元素的质量比为??????? ;
(2)混合物中钠元素的质量分数为??????? 。(精确至0.1%)
科目:初中化学 来源:1+1轻巧夺冠·优化训练 化学 九年级下册 (人教版) 银版 人教版 银版 题型:038
现有16.3 g由NaOH和NaCl组成的固体混合物,将它完全溶于一定量的水中,得50 g混合溶液,向该溶液中加入溶质质量分数为14.6%的稀盐酸50 g,恰好完全反应,得氯化钠溶液.求:
(1)所用盐酸中溶质的质量.
(2)原固体混合物中NaOH的质量.
(3)最终所得溶液的溶质质量分数.
查看答案和解析>>
科目:初中化学 来源:101网校同步练习 初三化学 人教社(新课标2001年通过) 人教实验版 题型:038
现有16.3 g由NaOH和NaCl组成的固体混合物,将它完全溶于一定量的水中,得50 g混合溶液,向该溶液中加入溶质质量分数为14.6%的稀盐酸50 g,恰好完全反应,得氯化钠溶液.求:
(1)所用盐酸中溶质的质量.
(2)原固体混合物中NaOH的质量.
(3)最终所得溶液的溶质质量分数.
查看答案和解析>>
科目:初中化学 来源:2008年江苏省常州市初中毕业升学统一考试、化学试卷 题型:038
某校化学兴趣小组为测定某硝酸铵样品的纯度,将10 g样品溶于30 g水后,再加入13.7 g氢氧化钠浓溶液共热,两者恰好完全反应(硝酸铵中的杂质不与氢氧化钠反应,也不溶于水,硝酸铵与氢氧化钠的反应方程式为:NH4NO3+NaOH![]() NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:
NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:

试回答下列问题:
(1)请在下面的坐标纸上,以反应时间为横坐标,以产生的NH3质量为纵坐标,画出能够表明产生气体的质量随时间变化的关系曲线;
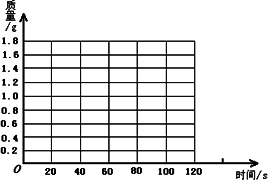
(2)表中m约为________;
(3)硝酸铵样品的纯度为________;
(4)试计算反应后所得硝酸钠溶液的溶质质量分数(不考虑反应过程中水损失的质量).
查看答案和解析>>
科目:初中化学 来源:2007年盐城市初中毕业升学统一考试 化学试题 题型:058
碳酸钠,化学式Na2CO3,俗称纯碱.“纯碱中常常会混有少量的氯化钠”.某研究性学习小组以一包纯碱(若有杂质,只考虑为氯化钠)为研究对象,探究该纯碱样品中碳酸钠的含量.请你参与他们的活动.
[小组讨论]
观点Ⅰ:纯碱样品中只含有碳酸钠
观点Ⅱ:纯碱样品是由碳酸钠和少量氯化钠组成的混合物
[实验设计]
甲方案
Ⅰ设计思路:根据样品与石灰水反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ操作步骤:称取13.25 g纯碱样品,加入过量的澄清石灰水,充分搅拌.过滤、洗涤、干燥,得到白色沉淀10.00 g
Ⅲ数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
Ⅳ实验结论:________.
乙方案
Ⅰ设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ实验结论:
(1)当a、b的质量关系满足________(填写含a、b字母的表达式,下同)时,纯碱样品中只含有碳酸钠,样品中碳酸钠的质量分数是100﹪.
(2)当a、b的质量关系满足________时,纯碱样品是由碳酸钠和少量氯化钠组成的混合物,样品中碳酸钠的质量分数是________.
[实验评价]
误差分析:(1)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.(2)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比________(填写“偏大”、 “偏小”或“不变”).
[交流反思]
(1)实验过程中,需用玻璃棒不断搅拌,该操作的目的是________.
(2)甲方案实验操作中,对沉淀洗涤的目的是:________.
(3)乙方案中,需用一定质量的19.6﹪的稀硫酸.现有一瓶98﹪的浓硫酸(密度为1.84 g/cm3),配制乙方案中实验所用稀硫酸,至少需要浓硫酸的体积是________mL(填写含字母的表达式).浓硫酸稀释的正确操作是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com