
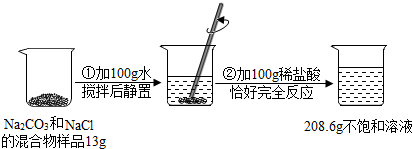
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
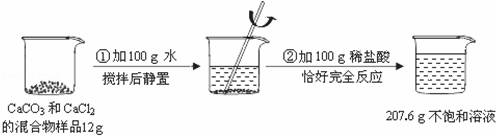
(1)该反应产生的气体质量为 g。
(2)实验所用稀盐酸的溶质的质量分数为 。
(3)计算原混合物样品中CaCl2的质量(写出计算过程)?
试题分析:(1)根据图中信息可以知道,反应前加入的物质的总质量为:12g+100g+100g=212g,而反应后剩余物质的总质量为207.6g,根据质量守恒定律可以知道物质减少的质量为生成二氧化碳的质量;
(2)利用生成的二氧化碳质量可以据化学方程式求出盐酸的质量分数;
(3)根据二氧化碳的质量结合化学方程式可以求算出碳酸钙的质量,进而可以求出氯化钙的质量.
解(1)反应中生成CO2的质量为:12g+100g+100g﹣207.6g=4.4g;
(2)设盐酸的质量分数为x,反应的碳酸钙质量是y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
y 100g×x 4.4g
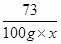 =
=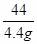 =
=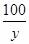
解得x=7.3%、y=10g
(3)由于混合物中碳酸钙的质量是10g,所以原混合物样品中CaCl2的质量为:12g﹣10g=2g


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| 加热 |
| ||
| 加热 |
| ||
| 二氧化锰 |
| ||
| 二氧化锰 |
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com