
下面是老师在同学们的作业本上发现的六个有问题的化学方程式:

⑤2C2H2+5O2====4CO2↑+2H2O
⑥CO2+Ca(OH)2====CaCO3+H2O(溶液变浑浊)
上述化学方程式中,化学式书写错误的是__________;“↑”或“↓”符号使用不当或遗漏的是__________;没有注明必要的反应条件的是_______;没有配平的是______。(以上空白均填写化学方程式的序号)
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
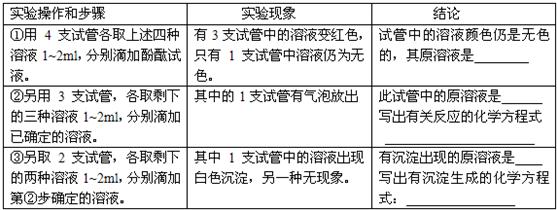
| 实验操作和步骤 | 实验现象 | 结论 |
| ①用4支试管各取上述四种溶液1~2ml,分别滴加酚酞试液. | 有3支试管中的溶液变红色,只有1支试管中溶液仍为无色. | 试管中的溶液颜色仍是无色的,其原溶液是 盐酸 |
| ②另用3支试管,各取剩下的三种溶液1~2ml,分别滴加已确定的溶液. | 其中的1支试管有气泡放出 | 此试管中的原溶液是 碳酸钠 |
| ③另取2支试管,各取剩下的两种溶液1~2ml,分别滴加第②步确定的溶液. | 其中1支试管中的溶液出现白色沉淀,另一种无现象. | 有沉淀出现的原溶液是 氢氧化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水以任意比互溶 |
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 NaOH NaOH 溶液 |
溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,和比色卡对照 | 溶液的pH小于7 | 猜想③成立 |
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中, 加入少量的NaOH溶液,然后将湿润的红色石蕊试纸放在试管口 加入少量的NaOH溶液,然后将湿润的红色石蕊试纸放在试管口 |
有刺激性气味的气体产生,红色石蕊试纸变蓝 有刺激性气味的气体产生,红色石蕊试纸变蓝 |
猜想④成立,该反应的化学方程式 (NH4)2SO4+2NaOH= Na2SO4+2NH3↑+2H2O (NH4)2SO4+2NaOH= Na2SO4+2NH3↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com