
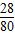 ×100%=35g.
×100%=35g. ×100%,则M×
×100%,则M×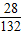 ×100%=35g.得M=165g.
×100%=35g.得M=165g.

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
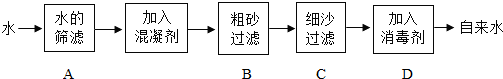
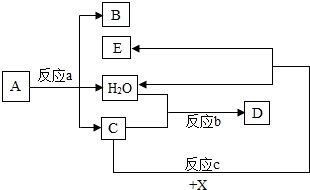
| 河段编号 | 水质类别 | 主要污染指标 | 质量状况 |
| 甲 | Ⅱ | 良好 | |
| 乙 | Ⅳ | 汞 | 一般 |
| 丙 | 劣Ⅴ | 总磷、氨(NH3 )氮等 | 较差 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com