
通过化学学 习,我们已经了解了常见金属在溶液中的活动性顺序。铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
习,我们已经了解了常见金属在溶液中的活动性顺序。铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
【提出假设】(1)对三种金属的活动性顺序提出三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如下:
| 金属 | Cr | Al | Cu |
| 与盐酸反应现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
【控制实验条件】(2)打磨三种金属发生的是 变化;上述实验使用等浓度的盐酸溶液的理由是 。
【得出结论】(3)原假设中正确的是 (填假设中“a”“b”或“c”)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式:
【结论应用】(4)根据探究结果,在CuCl2和AlCl3的混合液中加入一定量的金属铬,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有的溶质是 。
(1)由于金属铝的活动性比铜强,故金属铬的活动性与金属铝和铜相比较,有以下三种情况:①Al>Cr>Cu;②Cr>Al>Cu;③Al>Cu>Cr。(2)打磨金属的过程中,只是金属的形状发生改变,由于没有新的物质生成,故属物理变化;比较金属活动性顺序的实验中,只是金属不同,而其他的方面如温度、酸的浓度都应当相同。(3)根据三种金属与酸是否反应以及与酸反应的剧烈程度,可得出它们的活动性顺序。(4)向滤出的固体中加入盐酸不发生反应,说明加入的金属铬完全反应,溶液中的氯化铜可能恰好完全反应,也可能有剩余,而原溶液中的AlCl3由于不能被金属铬置换,存在于滤液中。
答案:(1)Al>Cu>Cr (2)物理 盐酸的浓度不同,会影响反应产生的气体的速率
(3)a Cr+2H Cl====CrC
Cl====CrC l2+H2↑
l2+H2↑
(4)CrCl2、AlCl3


科目:初中化学 来源: 题型:阅读理解
 环境保护是一个全球性的话题,作为对世界影响力最大的体育盛会--奥林匹克运动会,长期以来,在环保方面给世人留下的似乎是麻烦.2008年奥运,我国承诺“绿色奥运”.本次奥运会环保标志由人与绿树为主要形态.绿色的线条形如舞动的彩带,环绕交错,一笔描出,仿佛茂密的树冠,又似盛开的花朵,充满无限生机和希望,充分体现了自然环保的可持续性发展.树冠与人组成参天大树,代表着人与自然的和谐统一.
环境保护是一个全球性的话题,作为对世界影响力最大的体育盛会--奥林匹克运动会,长期以来,在环保方面给世人留下的似乎是麻烦.2008年奥运,我国承诺“绿色奥运”.本次奥运会环保标志由人与绿树为主要形态.绿色的线条形如舞动的彩带,环绕交错,一笔描出,仿佛茂密的树冠,又似盛开的花朵,充满无限生机和希望,充分体现了自然环保的可持续性发展.树冠与人组成参天大树,代表着人与自然的和谐统一.| 检测次数 | 废液中检测出的物质 |
| 第一次 | KNO3、Ba(NO3)2、Cu(NO3)2、HNO3 |
| 第二次 | KNO3、Ba(NO3)2、Mg(NO3)2、HNO3 |
| 第三次 | KNO3、Ba(NO3)2、AgNO3、HNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
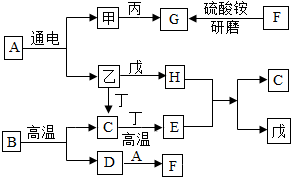 (2013?谷城县模拟)通过学习化学,我们了解了某些物质的性质以及物质之间的相互转化关系.如图中的物质均为初中化学常见的物质.其中甲、乙、丙、丁、戊均为单质,丙是空气中含量最多的物质;常温下,丁为黑色固体,戊为紫色金属;G是一种具有刺激性气味的气体,其水溶液显碱性,工业上用甲和丙化合制备G;农业上常用F改良土壤(如图中部分反应条件已省略).回答下列问题:
(2013?谷城县模拟)通过学习化学,我们了解了某些物质的性质以及物质之间的相互转化关系.如图中的物质均为初中化学常见的物质.其中甲、乙、丙、丁、戊均为单质,丙是空气中含量最多的物质;常温下,丁为黑色固体,戊为紫色金属;G是一种具有刺激性气味的气体,其水溶液显碱性,工业上用甲和丙化合制备G;农业上常用F改良土壤(如图中部分反应条件已省略).回答下列问题:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 物质 | 有利的一面(用途) | 不利的一面(危害) |
| 示例:氢气 | 可用作火箭推进剂 | 使用不当容易引起爆炸 |
二氧化碳气体 二氧化碳气体 |
能够促进绿色植物进行光合作用 能够促进绿色植物进行光合作用 |
一旦空气中含量过高,会导致温室效应 一旦空气中含量过高,会导致温室效应 |
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com