
将氯化钙和碳酸钙的混合物12g放入一个烧杯中,然后往其中加入123.4g稀盐酸,恰好完全反应,称量反应后剩余物质的总质量为131g.计算:
(1)生成二氧化碳的质量是多少?
(2)反应后所得溶液中溶质的质量分数是多少?
(1)4.4g (2)10%
【解析】
试题分析:(1)根据质量守恒定律,生成二氧化碳的质量=12g+123.4g﹣131g=4.4g;
(2)设原混合物中含有碳酸钙的质量为x,生成氯化钙的质量为y,则
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
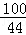 =
=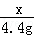 ,解得x=10g;
,解得x=10g;
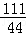 =
=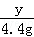 ,解得y=11.1g;
,解得y=11.1g;
反应后所得溶液中溶质的质量分数是 ×100%=10%.
×100%=10%.
答:(1)生成二氧化碳的质量是4.4g;
(2)反应后所得溶液中溶质的质量分数是10%.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.
点评:本题难度较大,主要考查了以化学方程式计算为基础,同时融入溶液等方面的计算题,这样的题目一直是中考的热点,主要培养学生的综合分析能力和计算能力.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源:2010年江苏省苏州市中考化学模拟试卷(八)(解析版) 题型:选择题
查看答案和解析>>
科目:初中化学 来源:2009年安徽省宣城市广德中学高中自主招生化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目:初中化学 来源:2009年北京实验外国语学校中考化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com