
①称量样品ag,称量前检查天平是否达平衡时,发现天平的指针向右偏转,则应将右边螺钉向________(填“左”或“右”)旋转,直到指针在标尺中间,否则实际称量的样品结果将________(填“大于”或“小于”)ag。
②溶解样品,溶解时需用玻璃棒搅拌,其目的是________。
③滴入稍过量的澄清石灰水,有关反应的化学方程式为:
Na2CO3+Ca(OH)2![]() CaCO3↓+2NaOH
CaCO3↓+2NaOH
检验澄清石灰水是否过量的方法是:静置溶液,向上层澄清液中滴入1~2滴________,观察是否有沉淀产生。
④过滤、洗涤、烘干沉淀,过滤时除需用铁架台(带铁圈)、烧杯、滤纸外,还要用到的仪器有________。洗涤、烘干沉淀,得bg固体。
⑤计算,氢氧化钠固体中碳酸钠的质量分数为________。
(2)在粗盐提纯的实验中有4次使用了玻璃棒,每次使用玻璃棒的目的分别是:
①________。②________。
③________。④________。
科目:初中化学 来源: 题型:
 20、化学兴趣小组测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量.
20、化学兴趣小组测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量.查看答案和解析>>
科目:初中化学 来源: 题型:
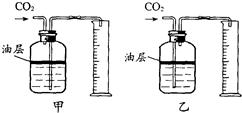 25、化学兴趣小组测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量.
25、化学兴趣小组测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量.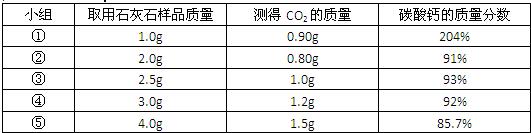
查看答案和解析>>
科目:初中化学 来源: 题型:
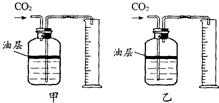
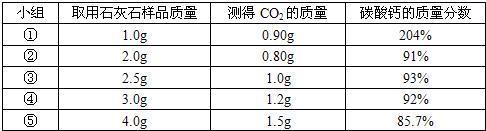
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验步骤 | 实验操作(说明仪器和试剂) | 实验现象 | 结论 |
| ① | 取少许粉末放入大试管中,再用滴管滴加 |
固体粉末 并有 |
仅除去铝 |
| ② | 再往大试管中加 |
固体 溶液 |
证明含有铁 |
| ③ | 将大试管静置,弃去上层清液,加水,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com