
| 12 |
| 44 |
| 2 |
| 18 |
| 1.8g |
| 12 |
| 0.4g |
| 1 |
| ||
| ||


科目:初中化学 来源: 题型:阅读理解
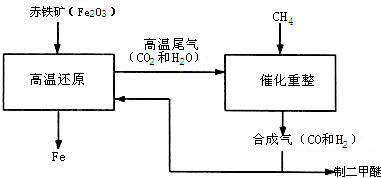
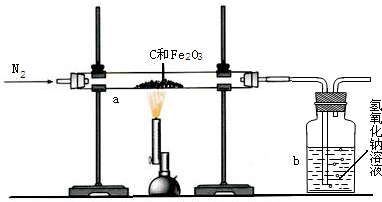
查看答案和解析>>
科目:初中化学 来源: 题型:
 某同学以右图所示的装置完成某化合物的组成分析实验,实验结果如下表所示:
某同学以右图所示的装置完成某化合物的组成分析实验,实验结果如下表所示:| 实验前 | 实验后 | |
| (铜的氧化物+玻璃管) 的质量 |
137.8g | 131.4g |
| (氯化钙+U形管) 的质量 |
100.8g | 108.0g |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
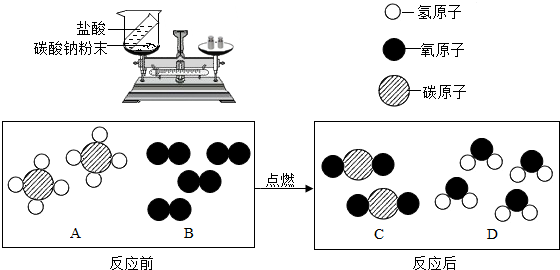
| 序号 | 反应前A的质量 | 反应前B的质量 | 反应后A3B2的质量 |
| ① | 8g | 2g | 6g |
| ② | 4g | 6g | 6g |
| ③ | xg | yg | 9g |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
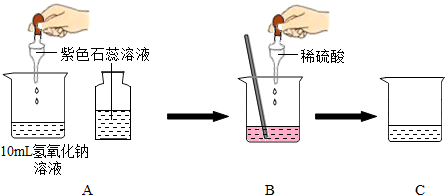
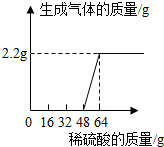
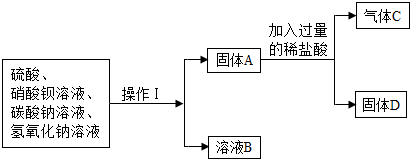
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com