
将Na2CO3和NaCl固体混合物22.3g放入烧杯中,加入182.1g稀盐酸恰好完全反应.待没有气泡溢出后,称量烧杯中剩余物质总质量为200g.请计算:
(1)生成二氧化碳的质量是 _________ ;
(2)求所得溶液中溶质的质量分数是多少?
(1)4.4g (2)11.7%
【解析】
试题分析:(1)反应生成二氧化碳的质量=22.3g+182.1g﹣200g=4.4g;故填:4.4g;
(2)设碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
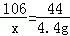
x=10.6g
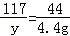
y=11.7g
所得溶液中溶质的质量分数=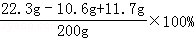 =11.7%
=11.7%
答:所得溶液中溶质的质量分数为11.7%.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.
点评:根据质量守恒定律,反应后所得溶液的质量=固体混合物的质量+稀盐酸的质量﹣生成二氧化碳气体的质量.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 实验步骤及操作方法 | 实验现象 | 结 论 |
| a、向装有滤液的烧杯中滴加 硝酸银溶液 |
有白色沉淀产生 有白色沉淀产生 |
假设③成立 |
| b、过滤后,向白色沉淀中加入足量的 稀硝酸 稀硝酸 . |
白色沉淀部分溶解,且有 气泡 气泡 产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 预期现象和结论 |
| 步骤1: 取少量的澄清滤液于试管中,然后向其中加入足量的硝酸钡溶液, 取少量的澄清滤液于试管中,然后向其中加入足量的硝酸钡溶液, |
①若产生白色沉淀,则含有碳酸钾; ②若无明显现象,则猜想④不正确; ①若产生白色沉淀,则含有碳酸钾; ②若无明显现象,则猜想④不正确; |
| 步骤2: 将步骤1中的溶液静置,然后取上层清液于试管中,然后向其中滴加酚酞试液 将步骤1中的溶液静置,然后取上层清液于试管中,然后向其中滴加酚酞试液 |
①若溶液变为红色,则含有氢氧化钾; ②若溶液不变色说明猜想④不正确; ①若溶液变为红色,则含有氢氧化钾; ②若溶液不变色说明猜想④不正确; |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com