
某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物。
(一)K2SO4的制备

(1)将CaCO3研成粉末的目的是___________________________________。
(2)M物质的化学式为__________。
(3)反应Ⅲ中相关物质的溶解度如下表。
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
反应Ⅲ在常温下能实现的原因是_______________________________________。
(4)上述流程中可循环使用的物质有CO2和_____________(填写化学式)。
(二)研究CaSO4•2H2O加热分解的产物
(5)分离出的CaSO4•2H2O中常含有CaCO3,可用盐酸除去CaCO3,
该反应的化学方程式_______________________________________________。
(6)为了测定CaSO4•2H2O和CaCO3的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验。注:碱石灰的主要成分为NaOH和CaO。

① 实验前首先要________________,再装入样品。装置A的作用是_________________。
② 已知:CaSO4•2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解; CaCO3在900℃时分解完全。
现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将______。(填“偏大”、“偏小”或“无影响”)你认为还可选用上述的________________(选填序号)两个数据组合也可求出x:y的值。
(7)CaSO4•2H2O受热会逐步失去结晶水。取纯净CaSO4•2H2O固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示。

则G点固体的化学式是_________________。
加快反应速率(或使反应更充分或提高原料的利用率等合理答案均给分) (NH4)2SO4 常温下K2SO4的溶解度小 CaCO3 CaCO3+2HCl=CaCl2+CO2↑+H2O 检查装置的气密性 除去空气中的CO2和H2O 偏小 b、c CaSO4•H2O 【解析】(一)(1)根据将CaCO3研成粉末,碳酸钙与硫酸接触面积更大,其目的是加快反应速率解答;(2)根据质量守恒定律分析解答;(3)... 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:初中化学 来源:福建省泉州市2018届九年级上学期教学质量检测化学试卷 题型:填空题
水和水溶液是人类必不可少的物质。
(1)科学家对水的生成和分解实验的研究,确认了水是由______和______组成的。
(2)自然界中的水都不是纯水,利用沉淀、_______、吸附和蒸馏等方法可以净化水。
(3)生活中简便区别硬水和软水的方法是_______________。
(4)下图为甲乙两物质的溶解度曲线。
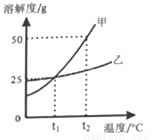
①t2℃时,溶解度较大的物质是_________。
②t1℃时,乙物质饱和溶液中溶质的质量分数为________。
③t2℃时,将50g甲物质放入50g水中,充分溶解后,发现有未溶解的甲物质,其质量是______g。
(1)水能灭火,但有时水也能“生火”。比如将过氧化钠(Na2O2)用脱脂棉包裹,再向上面滴加水,脱脂棉一会儿就会发生燃烧。该反应的化学方程式为:2Na2O2+2H2O═4NaOH+X↑。
①X的化学式是______。
②包裹过氧化钠的脱脂棉滴水后,引起脱脂棉能燃烧起来的原因是________。
氢元素(或H) 氧元素(或O) 过滤 分别取样,加入肥皂水,搅拌,产生泡沫很少且有白色垢状物形成的水为硬水 甲 20% 25 O2 过氧化钠与水反应放出热量,使脱脂棉的温度达到着火点且产生大量氧气 【解析】(1)物质是由元素组成的,是由科学家对水的生成和分解实验的研究,确认了水是由氢元素和氧元素组成的; (2)自然界中的水都不是纯水,利用沉淀、过滤、吸附和蒸馏等方法可以净化水; ...查看答案和解析>>
科目:初中化学 来源:陕西省2018年中考化学试卷 题型:科学探究题
化学兴趣小组的同学按图示装置及步骤验证氢氧化钠的化学性质。
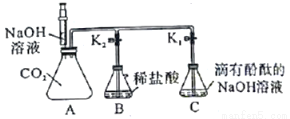
(实验步骤)
I.将注射器内的液体注入A中的锥形瓶。
II.打开K1,观察到C中部分红色溶液沿导管倒吸入A,片刻后回流停止。
III.打开K2,观察到B中溶液倒吸入A、C中,液面稳定后观察到A中溶液仍为红色,C中溶液变为无色。
同学们对相关问题分组展开如下探究。
探究环节 | 甲组的探究 | 乙组的探究 |
[提出问题] | A中使酚酞变为红色的物质是什么? | C中溶液为什么变成无色? |
[做出猜想] | 猜想一:Na2CO3 猜想二:Na2CO3和NaOH | 猜想一:实验过程中酚酞变质了 猜想二:溶液中的NaOH反应完了 |
[实验验证] | 小鹏取少量A中溶液于试管中,向其中滴加过量BaCl2溶液,若观察到______,证明猜想二成立。小丽认为用Ba(OH)2溶液也可证明猜想二成立,小鹏认为小丽的方案不合理,理由是_______。 | (1)取少量C中溶液于试管中,向其中滴加NaOH溶液. 溶液又变为红色,证明猜想一不成立。 (2)用pH试纸测定C中溶液的酸碱度,若pH___7,证明猜想二成立。 |
(反思交流)(1)甲、乙两组同学的实验证明了NaOH能与稀盐酸、CO2发生反应;A中溶液里一定还存在NaCl。写出NaOH与CO2发生反应的化学方程式_________。
(2)[实验步骤]中的现象_____(填“能”或“不能”)证明NaOH与CO2发生了反应。
(拓展迁移)对于无明显现象的化学反应,可通过检验有新物质生成或检验_____的方法来证明反应发生了。
(甲组)生成白色沉淀,溶液仍为红色; 向溶液中引入OH-,对NaOH的检验产生干扰。 ≤(或<或=) 2NaOH+CO2=Na2CO3+H2O 不能; 某种反应物消失(或减少) 【解析】[实验验证] (甲组)根据Na2CO3与BaCl2溶液会反应生成碳酸钙沉淀,溶液酸碱性不变解答;根据向溶液中引入OH-,对NaOH的检验产生干扰解答;(乙组)根据溶液显酸性或中性,pH≤7解答;【反思交流...查看答案和解析>>
科目:初中化学 来源:福建省泉州市五校2018届九年级联考模拟化学试卷 题型:简答题
化学来源于生活,服务于生活。请回答下列生活中的有关问题:
(1)从化学与健康角度:
① 当人体中缺少某些元素时会影响健康,人体缺铁会引起__________;
② 下列做法不会危害人体健康的是__________(填字母序号)。
A.用碳酸氢钠焙制糕点 B.在奶粉中添加化工原料三聚氰胺
C.用工业石膏或医疗废弃石膏制作豆腐 D.把霉变的花生榨油用于食用
(2)从化学与能源角度:
① 天然气是我们日常生产生活中常用的化石燃料之一。
天然气属于____(填“可再生”或“不可再生”)能源,天然气完全燃烧的化学方程式为___。
② 你知道的新能源有哪些?_____________(任写一种)
(3)从化学与材料角度:
① 衣服用料中的羊毛属于______(填“天然纤维”或“合成纤维”);
② 生铁和钢都是铁合金,它们的性能不同的原因是__________________________。
③ 合金的很多性能与组成它们的纯金属不同。如图中能表示锡铅合金的是_______(填序号“a”、“b”或“c”)。
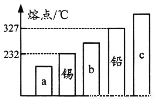
④ 镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是_________________任写一个化学方程式)。该合金是一种储氢材料,完全吸氢后得到MgH2和Al, “储氢过程”属于__________(填“物理”或“化学”)变化。
(4)从化学与环境角度:
烟道气中含有大量CO2,经“捕捉”可用于生产甲醇(CH3OH)等产品。
①“捕捉”CO2:在高压时将烟道气中的CO2溶解于甲醇,得到CO2的甲醇溶液。所得溶液中溶质是___________。
② 用“捕捉”的CO2生产甲醇,反应的微观示意图如下:

该反应的化学方程式为____________________________________。
贫血 A 不可再生 CH4+2O2点燃2H2O+CO2 太阳能(合理即可) 天然纤维 含碳量不同 a 2Mg+O2=2MgO(或4Al+3O2=2Al2O3) 化学 CO2 CO2+3H2CH3OH+H2O 【解析】(1)①根据铁的生理功能解答;②根据物质的性质分析解答;(2)①根据天然气的形成及主要成分甲烷与氧气在点燃的条件下反应生成二氧化碳和水解答;②根据太阳能、风能等属于新能源解答;(...查看答案和解析>>
科目:初中化学 来源:福建省泉州市五校2018届九年级联考模拟化学试卷 题型:单选题
玻璃棒是化学实验中常用的仪器,下列实验过程中一般不需要使用玻璃棒的是( )
A. 配制5%的稀硫酸溶液 B. 除去悬浮于水中的不溶物
C. 从氯化钠溶液中得到氯化钠固体 D. 用量筒量取50mL的水
D 【解析】A、配制5%的稀硫酸溶液,进行稀释时,应用玻璃棒进行搅拌,错误;B、除去悬浮于河水中的不溶物的操作是过滤,过滤时应使用玻璃棒进行引流,错误;C、从氯化钠溶液中得到氯化钠固体,应采用蒸发的方法,蒸发时应使用玻璃棒进行搅拌,错误;D、用量筒量取50mL水,应使用量筒和胶头滴管,无需使用玻璃棒,正确。故选D。查看答案和解析>>
科目:初中化学 来源:福建省泉州五校2018届九年级联考模拟卷化学试卷 题型:单选题
草酸(H2C2O4)是一种有机酸,其水溶液呈酸性。它广泛分布于植物、动物和真菌体中,并在不同的生命体中发挥不同的功能。下列有关草酸的叙述正确的是( )
A. 其中碳元素的化合价为+4 B. 氢元素和氧元素的质量比为1:32
C. 一个草酸分子由8个元素组成 D. 其溶液中滴加酚酞试液时呈红色
B 【解析】A、化合物中元素的化合价的代数和为零,设碳元素的化合价为x,则2x+(+1)×2+(-2)×4="0," x=+3;B、化合物中元素的质量比=(相对原子质量×原子个数)之比,氢元素和氧元素的质量比为2:4×16=1:32;C.化学式中元素右下角的数字为一个分子中原子的个数,所以一个草酸分子由8个原子构成; D.酸性溶液中滴加酚酞试液时,呈无色;选B查看答案和解析>>
科目:初中化学 来源:福建省泉州五校2018届九年级联考模拟卷化学试卷 题型:单选题
规范的操作是实验成功的前提,下列实验操作正确的是( )
A. 实验完毕后,实验过程中剩余的试剂都应该放回原试剂瓶
B. 蒸发饱和食盐水,蒸发皿必须放在石棉网上,用酒精灯的外焰加热
C. 玻璃管与胶皮管连接时,应将玻璃管一端用水润湿,稍用力转动插入胶皮管中
D. 没有腐蚀性的药品可直接放在电子秤上称量,有腐蚀性的应放在烧杯中称量
C 【解析】A、实验完毕后,实验过程中剩余的试剂不能放回原试剂瓶,因为会污染原瓶中的药品,错误;B、蒸发皿可以直接加热,不需要垫石棉网,错误;C、玻璃管与胶皮管连接时,将玻璃管一端用水润湿,稍用力转动插入胶皮管中,正确;D、没有腐蚀性的药品直接放在天平上称量会污染药品,应垫上一张纸,错误。故选C。查看答案和解析>>
科目:初中化学 来源:湖北省荆州市毕业班调研考试化学试卷 题型:单选题
食用“染色”馒头会对人体造成危害。已知铬酸铅PbCrO4中铅元素的化合价为+2价,则铬元素(Cr)的化合价为( )
A. +6 B. +4 C. +2 D. +1
A 【解析】铬酸铅的化学式为PbCrO4,其中铅元素的化合价为+2价,氧元素的化合价为-2价,设铬元素的化合价为x,根据化合价的代数和为0,+2+x+(-2)4=0,得x=+6价,故选A。查看答案和解析>>
科目:初中化学 来源:湖北省2018届九年级5月月考化学试卷 题型:填空题
如图是甲、乙、丙三种物质的溶解度曲线。

(1) 甲的溶解度为25g时的温度为_________。
(2) t3℃时,甲、乙各50g,分别加入到100g水中,充分搅拌。其中,不能形成饱和溶液的是_____。
(3) t3℃时,甲的饱和溶液中含有少量的丙,现要提纯甲可采用的结晶方式是____________
(4) 下列说法正确的是_________
A. 将甲、乙的饱和溶液分别从t1℃升温到t2℃,溶质的质量分数都不变
B. t2℃时,向100g甲的饱和溶液中加100g水,充分搅拌,溶液的浓度为10%
C. t3℃时,等质量的甲、乙、丙分别制成饱和溶液,需水的质量最多的是甲
D. 升高丙的饱和溶液的温度,一定有晶体析出
t2; 甲,; 降温结晶; ABD 【解析】(1) 在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。甲的溶解度为25g时的温度为t2;(2) 溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。 t3℃时,甲的溶解度大于50g,乙的溶解度小于50g,甲、乙各50g,分别加入到100g水中,充分搅拌。甲不能形成饱和溶液;(3)甲的溶解度随温度的降低迅速减小,而丙的溶解度随温度降低...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com