
| 111 |
| x |
| 6 |
| 2.46g-2.4g |
| 1.11g |
| 2.4g |


科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
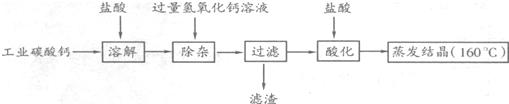
2008年春节前夕,我国南方有些地区遭遇冰雪灾害。为了清除道路上的冰雪,有关部门投入了大量工业盐融雪剂用于除冰。同学们从资料中得知:①使用工业盐融雪剂后,道路两旁的树木、农作物大量死亡![]() ;②桥梁路面除冰不得使用工业盐融雪剂。
;②桥梁路面除冰不得使用工业盐融雪剂。
【提出问题】工业盐融雪剂为什么会对树木、农作物和桥梁造成危害?
【查找资料】(1)工业盐的主要成分是NaCl和NaNO2;(2)土壤盐碱化会造成树木、农作物死亡。
【作出猜想】猜想一:工业盐溶液可能显碱性;
猜想二:工业盐溶液对钢铁可能有更强的腐蚀性。
【实验探究】请你填空:
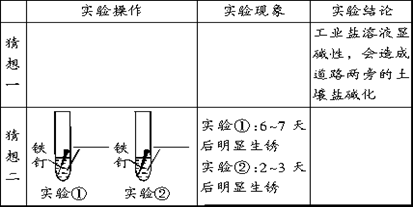 【反思与应用】 对于道路除冰,请你提出更好的建议___________________。
【反思与应用】 对于道路除冰,请你提出更好的建议___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
融雪剂可以融化道路上的积雪。某种融雪剂由氯化钠和氯化钙组成,为测定该融雪剂中氯化钙的质量分数,称量2.4 g融雪剂放入烧杯中,加足量水使其完全溶解,再加入碳酸钠溶液至恰好完全反应,过滤后,将滤液蒸干得到2.46 g固体。求融雪剂中氯化钙的质量分数。
已知:Na2CO3 + CaCl2 === CaCO3↓ + 2NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com