
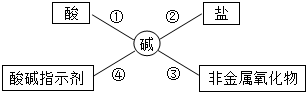
 酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题:
酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题:分析 (1)根据氢氧化钠能够吸收空气中的二氧化碳,并且能够反应生成碳酸钠和水解答;
(2)根据氢氧化钠变质,氢氧化钠溶液中就含有碳酸钠,碳酸钠显碱性,只要能证明溶液中是否含有碳酸根离子就能判断氢氧化钠溶液是否变质;
(3)根据碱中都含有氢氧根离子解答;
(4)根据复分解反应发生的条件解答;
(5)根据复合肥是含有两种或两种以上营养元素的化肥解答.
解答 解:(1)氢氧化钠和二氧化碳发生反应生成碳酸钠和水,化学方程式为:2NaOH+CO2═Na2CO3+H2O;
(2)A、滴加盐酸,有气泡生成,说明溶液中含有碳酸钠,因此盐酸能验证氢氧化钠溶液已变质,故选项不符合题意;
B、氢氧化钠变质,氢氧化钠溶液中含有碳酸钠,碳酸钠也显碱性,也能使酚酞试液变红色,因此无色酚酞不能验证氢氧化钠溶液已变质,故选项符合题意;
C、滴加氯化钙溶液,有白色沉淀生成,说明溶液中含有碳酸钠,因此氯化钙溶液能验证氢氧化钠溶液已变质,故选项不符合题意;
D、滴加氢氧化钙溶液,有白色沉淀生成,说明溶液中含有碳酸钠,因此氢氧化钙溶液能验证氢氧化钠溶液已变质,故选项不符合题意.
(3)碱中都含有氢氧根离子,无色酚酞试液分别滴入NaOH溶液和澄清石灰水中,溶液由无色变成红色,原因是它们在水溶液中能电离出OH-;
(4)依据反应②,碱可以和盐反应;
A、H2SO4 是酸;
B、BaCl2是盐,和KOH相互交换成分没有气体、沉淀和水生成,不反应;
C、CuSO4 是盐,和KOH相互交换成分有氢氧化铜蓝色沉淀生成,反应;
D、Na2CO3是盐,和KOH相互交换成分没有气体、沉淀和水生成,不反应;
发生反应的化学方程式为:CuSO4+2KOH=K2SO4+Cu(OH)2↓.
(5)硫酸铵[(NH4)2SO4]、磷酸二氢钙[Ca(H2PO4)2]、亚硝酸钠(NaNO2)、硝酸钾(KNO3)等属于盐,其中又属于复合肥的是硝酸钾(KNO3),既含有甲元素,有含有氮元素.
答案:(1)2NaOH+CO2═Na2CO3+H2O;
(2)B;
(3)OH-;
(4)C CuSO4+2KOH=K2SO4+Cu(OH)2↓;
(5)硝酸钾(KNO3).
点评 本题主要考查NaOH的化学性质和碳酸盐的检验,难度不大,是对所学知识的综合运用,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力,学习中全面把握基础知识.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 A~J都是初中化学中的常见物质,它们之间的关系如图所示(图中省略了反应条件,部分反应物或部分生成物),图中”→“表示箭尾的物质可转化成箭头的物质;”-“表示两端的物质能发生化学反应,”
A~J都是初中化学中的常见物质,它们之间的关系如图所示(图中省略了反应条件,部分反应物或部分生成物),图中”→“表示箭尾的物质可转化成箭头的物质;”-“表示两端的物质能发生化学反应,” “表示两端的物质能发生化学反应,又表示箭尾的物质可转化成箭头的物质;”?“表示两端物质间可互相转化,A是天然气的主要成分,I、H是两种常见的金属(其中金属I的颜色为红色).③和⑦的反应物质均为置换反应(形如AB+C→CB+A).请回答下列内容
“表示两端的物质能发生化学反应,又表示箭尾的物质可转化成箭头的物质;”?“表示两端物质间可互相转化,A是天然气的主要成分,I、H是两种常见的金属(其中金属I的颜色为红色).③和⑦的反应物质均为置换反应(形如AB+C→CB+A).请回答下列内容查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究.
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究.| 实验编号 | 1 | 2 |
| 反应物 | 6%H2O2 | 6%H2O2 |
| 催化剂 | 1g红砖粉 | 1gMnO2 |
| 时间 | 152秒 | 35秒 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁和硫酸铜溶液 | B. | 氧化铁固体和稀硫酸 | ||
| C. | 盐酸和澄清石灰水 | D. | 氯化钠溶液和硝酸钾溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 设计了如图所示的实验:一个密封的饮料瓶装有二氧化碳气体,然后用注射器向瓶内注入100mL的水,实验过程中始终保持密封.请你根据生活经验及所学的知识,结合实验回答下列问题:
设计了如图所示的实验:一个密封的饮料瓶装有二氧化碳气体,然后用注射器向瓶内注入100mL的水,实验过程中始终保持密封.请你根据生活经验及所学的知识,结合实验回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含有氧元素的化合物称为氧化物 | |
| B. | 同种元素组成的物质一定是纯净物 | |
| C. | 质子数相同的粒子一定是同种元素 | |
| D. | 多种元素形成的纯净物一定是化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不能用铜和稀硫酸反应制取氢气 | |
| B. | 相同条件下,锌和铁的与稀硫酸反应的剧烈程度 | |
| C. | 铁能置换出硫酸铜溶液中的铜 | |
| D. | 在化合物中,铁显+2、+3价,铜显+1、+2价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com