
将5 mL密度为1.84 g/cm3的98%的浓硫酸加入到10 mL水中,所得溶液中溶质的质量分数的算式正确的是
A.![]()
B.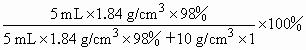
C.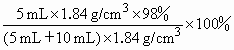
D.
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 加入盐酸体积V/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度上升(t)/℃ | 15.2 | 19.6 | 22.0 | 26.0 | 28.2 | 26.7 | 25.7 | 24.7 | 23.7 | 22.9 |

| 实验方法 | 可能观察到的现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源:江苏省常州市部分学校2011届中考模拟联考化学试题 题型:058
甲、乙两个实验小组分别进行“Na2CO3和NaCl混合物中Na2CO3含量测定”的实验:
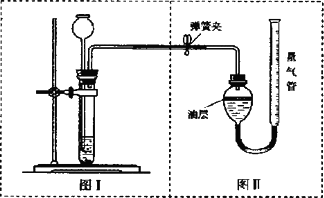
(1)检查图Ⅱ气密性的方法是________.
(2)甲组的方法是:用已知浓度盐酸滴加到一定质量的混合物,根据消耗盐酸溶液的体积来测定碳酸钠的含量.在实验过程中除盐酸、试样与水以外,判断反应是否完全必须用到的试剂是
________.(3)乙组的方法是:将样品与稀盐酸反应,测定反应后生成CO2的体积,经换算并计算出样品中Na2CO3的质量.用右图装置测定产生的CO2气体的体积,请分析图Ⅱ装置中油层的作用是
________;使反应前后油层上方气体压强和外界大气压相同的操作方法是________.(4)用200 mL密度为1.2 g·mL-1质量分数为38%的浓盐酸,配制10%密度为1.02 g·mL-1的稀盐酸,需要水________mL.
(5)若取用Na2CO3和NaCl的混合物6.2 g,加入某浓度的稀盐酸96 g恰好反应,图Ⅱ收集到二氧化碳1100 mL,此时二氧化碳的密度为2 g·L-1,求①收集到二氧化碳多少克?②混合物中碳酸钠的质量③反应后溶液中溶质的质量分数.(③保留3位有效数字)
(6)请你再设计一个与甲、乙组操作不同的实验方法,测定混合物中的Na2CO3含量.你选用的药品是________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com