
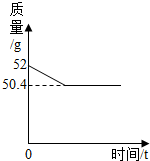
为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示。

(1)反应完全后产生氧气的质量为
(2)欲从反应后的混合物中回收二氧化锰,应进行的操作是 、干燥。
(3)计算该过氧化氢溶液中溶质的质量分数(结果保留至0.1%)。
(1)1.6
(2)过滤
(3)设溶液中H2O2的质量为x。
2H2O2MnO22H2O+O2↑
68 32
x 1.6g
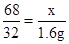
x=3.4g
该过氧化氢溶液中溶质的质量分数为: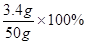 =6.8%
=6.8%
答:该过氧化氢溶液中溶质的质量分数为6.8%。
【解析】
试题分析:(1)依据图像数据,结合根据质量守恒定律,氧气的质量为反应前物质的质量-
反应后物质的质量=502g-50.4g=1.6g;(2)二氧化锰不溶于过氧化氢和水,故分离时可采用过滤的方法;(3)用氧气的质量可求出过氧化氢的质量,再用过氧化氢的质量除以过氧化氢溶液的质量乘以100%就是过氧化氢溶液中溶质的质量分数。
考点:质量守恒定律和化学计算。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示.
为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com