
| 实验 | 第一次 | 第二次 | 第三次 |
| 取用黄铜样品质量/g | 2 | 2 | 4 |
| 加入稀硫酸质量/g | 20 | 25 | 20 |
| 充分反应后过滤得固体质量/g | 0.8 | 0.8 | 2.8 |
| 1.2g |
| 2g |
| 65 |
| 1.2g |
| 98 |
| x |
| 1.8g |
| 20g |


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
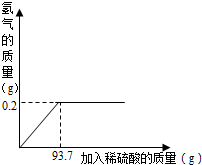 我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取10g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示.请解答下列问题:
我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取10g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示.请解答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 连续加入盐酸的质量/g | 20 | 20 | 20 | 20 |
| 生成氢气的质量/g | 0.08 | 0.08 | 0.04 | ? |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?黑龙江)黄铜是铜和锌的合金,可以用来制造机器、电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取20g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示.
(2012?黑龙江)黄铜是铜和锌的合金,可以用来制造机器、电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取20g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com