21 假设氧气全部反应,除氧气外,被消耗的气体体积占集气瓶容积的9%,所以被消耗气体占空气的体积分数一定超过9%,只有氮气符合要求 氮气 镁条能在氮气中燃烧 -3 3Mg+N
2
Mg
3N
2 2Mg+CO
2
C+2MgO 燃烧不一定非要有氧气参加
分析:空气成分探究实验的变形,把熟悉红磷换成了性质活泼的金属镁,药品的更换而使实验中的现象出现异常,对异常现象的分析及造成异常现象出现原因的分析,生成了对燃烧的重新认识.
解答:【发现问题】若镁条象红磷一样,只消耗空气中的氧气,则此探究实验会得出和使用红磷一样的实验结果:进入水的量不超过空气中氧气所占的体积分数21%;可现进入集气瓶中水的体积约为其容积的30%,假设氧气全部反应,除氧气外,被消耗的气体体积占集气瓶容积的9%,所以被消耗气体占空气的体积分数一定超过9%,只有氮气符合要求
故答:21;假设氧气全部反应,除氧气外,被消耗的气体体积占集气瓶容积的9%,所以被消耗气体占空气的体积分数一定超过9%,只有氮气符合要求;氮气;
【实验结论】把点燃的镁条伸进含有剩余气体的集气瓶中,发现镁条能在余下的气体中剧烈燃烧,说明镁条能在氮气中燃烧.故答案为:镁条能在氮气中燃烧;
【查阅资料】①根据氮化镁的化学式Mg
3N
2计算其中N元素化合价,根据化合物中正负元素化合价代数和为零,镁为+2价,假设N元素化合价为x,则有:(+2)×3+2x=0,解得x=-3;镁条在氮气中能燃烧并生成氮化镁(Mg
3N
2)固体,反应的化学方程式3Mg+N
2
Mg
3N
2.故答案为:-3;3Mg+N
2
Mg
3N
2;
②镁在二氧化碳气体中燃烧生成碳和氧化镁,该反应的化学方程式是2Mg+CO
2
C+2MgO;故答案为:2Mg+CO
2
C+2MgO;
【实验反思】通过以上探究,可以得出燃烧不一定非要有氧气参加;故答案为:燃烧不一定非要有氧气参加.
点评:实验室探究空气成分不选择镁做燃料,因为镁条燃烧时不但消耗氧气而且还会消耗空气中的氮气.

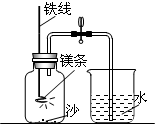 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹. Mg3N2 2Mg+CO2
Mg3N2 2Mg+CO2 C+2MgO 燃烧不一定非要有氧气参加
C+2MgO 燃烧不一定非要有氧气参加 Mg3N2.故答案为:-3;3Mg+N2
Mg3N2.故答案为:-3;3Mg+N2 Mg3N2;
Mg3N2; C+2MgO;故答案为:2Mg+CO2
C+2MgO;故答案为:2Mg+CO2 C+2MgO;
C+2MgO;

 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%. 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验.先将镁条燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验.先将镁条燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹.