
科目: 来源:不详 题型:计算题
| | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.生成铁的氯化物质量为12.7 g | B.生成铁的氯化物质量为95.0 g |
| C.生成铁的氯化物为FeCl2 | D.生成铁的氯化物为FeCl3 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
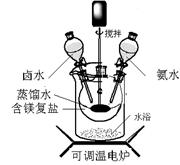
| 实验操作 | 实验现象 | 实验结论 |
| ①取样溶解,向样品溶液中滴加过量稀硝酸。 ②再向上述所得溶液加 溶液 | 现象① ; 现象② ; | 含有 Cl- |
|
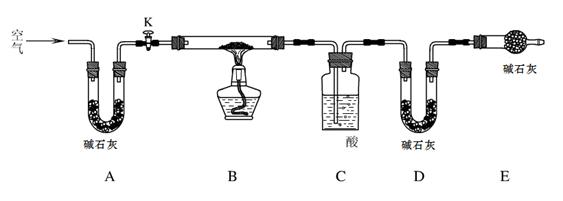
查看答案和解析>>
科目: 来源:不详 题型:计算题
| | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
| 生成沉淀的质量/g | 2.9 | x | 8.7 | 8.7 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
查看答案和解析>>
科目: 来源:不详 题型:计算题
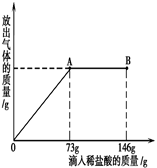
查看答案和解析>>
科目: 来源:不详 题型:计算题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶 解 度 /g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2SO4 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| CaCl2 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| MgCl2 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |



查看答案和解析>>
科目: 来源:不详 题型:计算题
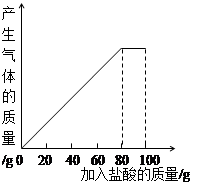
| 次数 | 第一次 | 第二次 | 第三次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 25 | a | 15 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.56% | B.37.5% | C.36% | D.55% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com