
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 在实验室里,某同学看到氢氧化钠试剂瓶的瓶口有白色粉末,如图所示:
在实验室里,某同学看到氢氧化钠试剂瓶的瓶口有白色粉末,如图所示: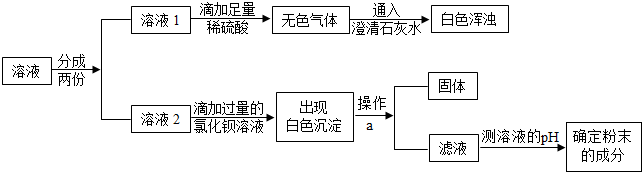
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
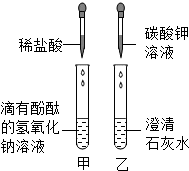 某校研究学习小组的同学在探究复分解反应发生的条件时,进行了如图所示的实验.
某校研究学习小组的同学在探究复分解反应发生的条件时,进行了如图所示的实验.| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量的氯化钙溶液,静置. | ①有白色沉淀产生,溶液由红色变无色. | |
| ② |
查看答案和解析>>
科目: 来源: 题型:
| ||
| △ |
查看答案和解析>>
科目: 来源: 题型:
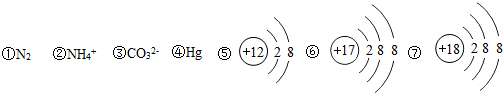
查看答案和解析>>
科目: 来源: 题型:
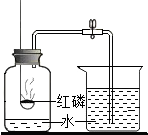 某班同学用右图装置测定空气里氧气的含量.先用弹簧夹夹住橡皮管.点燃红磷伸入瓶中并塞上瓶塞.待红磷熄灭后,打开弹簧夹,观察广口瓶内水面变化情况.
某班同学用右图装置测定空气里氧气的含量.先用弹簧夹夹住橡皮管.点燃红磷伸入瓶中并塞上瓶塞.待红磷熄灭后,打开弹簧夹,观察广口瓶内水面变化情况.| 1 |
| 5 |
查看答案和解析>>
科目: 来源: 题型:
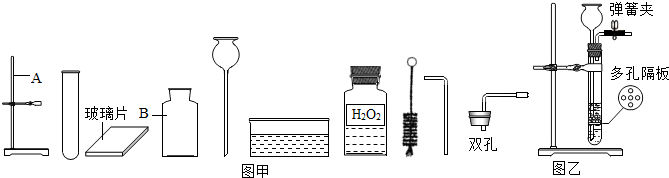
| 实验 步骤 | a.制备气体 | b.收集气体 | c.检查装置气密性 | d.清洗仪器、整理桌面 |
| 相关 实验 装置 | 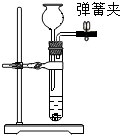 |  | 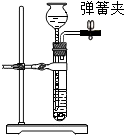 |  |
查看答案和解析>>
科目: 来源: 题型:
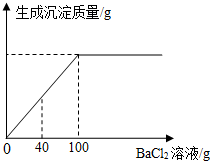 小张同学为了测定某混合物(含Na2CO3和NaOH)中碳酸钠的质量分数.进行了如下实验:现称取了该样品20g配成溶液,然后向该溶液中逐滴加入溶质质量分数为20.8%的BaCl2溶液,生成沉淀的质量与加入BaCl2溶液的质量关系如图所示.
小张同学为了测定某混合物(含Na2CO3和NaOH)中碳酸钠的质量分数.进行了如下实验:现称取了该样品20g配成溶液,然后向该溶液中逐滴加入溶质质量分数为20.8%的BaCl2溶液,生成沉淀的质量与加入BaCl2溶液的质量关系如图所示.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com