兴趣小组同学为了探究实验室中久置的氢氧化钠固体是否变质及变质程度,进行了有关实验.请你与他们一起完成以下探究活动.
【对氢氧化钠固体猜想】
猜想Ⅰ:该氢氧化钠固体没有变质;
猜想Ⅱ:该氢氧化钠固体部分变质;
猜想Ⅲ:
.
【实验和推断】
①小华同学取一定量该氢氧化钠固体样品加入适量水配成2mL溶液,然后向其中投入0.2g的熟石灰粉末,振荡,观察到有白色不溶物,于是小华就得出猜想Ⅰ不成立的结论.小明认为小华的实验不严密,其理由是
.
②经过同学们讨论,大家一致认为只要取一定量该氢氧化钠固体样品加入适量水配成溶液,然后向溶液中加入两种试剂就能验证三种猜想.其实验过程:
取少量该溶液于试管中,加入
溶液,静置后,在上层清液中,滴加2~3滴
,观察现象.
若经过实验证明猜想Ⅱ成立,则实验中观察到的实验现象是
.
【Na
2CO
3含量的测定】同学们经过实验发现该氢氧化钠固体已部分变质,该化学兴趣小组欲探究该氢氧化钠固体中Na
2CO
3的质量分数
(1)该兴趣小组的同学设计了如图所示的实验装置.取10.0g氢氧化钠固体样品,进行实验.
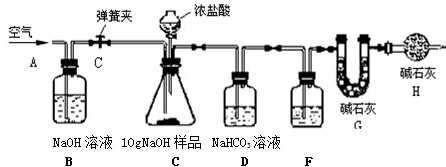
【说明】①碱石灰是CaO与NaOH的固体混合物.
(2)操作步骤:
①连接好装置,检查气密性;
②打开弹簧夹C,在A处缓缓通入一段时间空气;
③称量G的质量;
④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;
⑤打开弹簧夹C,再次缓缓通入一段时间空气;
⑥再次称量G的质量,得前后两次质量差为4.4g.
(3)问题探究:
①F中的试剂应为
.
②B装置的作用是
,H装置的作用是
.
(4)数据计算:该氢氧化钠样品中Na
2CO
3的质量分数为
%.
(5)反思与评价:
请你仔细分析此次实验并结合所求出的该氢氧化钠样品中Na
2CO
3的质量分数,对此次实验进行评价
;如果此次实验存在不足之处请你提出改进的方法
.(如果此次实验不存在不足之处,此空格不要填写)
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示)
【拓展应用】有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出的二氧化碳气体的质量与加入稀盐酸的质量关系如图所示.试求:10g样品与足量的稀盐酸反应后生成氯化钠的质量是多少克?
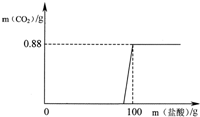
答:


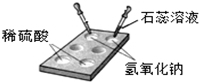 (1)如图所示,在白色点滴板上进行实验,探究酸和碱化学性质的实验中使用的白色点滴板,实验时它的优点有
(1)如图所示,在白色点滴板上进行实验,探究酸和碱化学性质的实验中使用的白色点滴板,实验时它的优点有
