
科目: 来源: 题型:
轻质碳酸钙广泛应用于橡胶、塑料、油漆、水性涂料以及造纸等行业,日常生活中的牙膏也常用它作摩擦剂。目前轻质碳酸钙的生产主要是碳化法,工艺流程见下图:
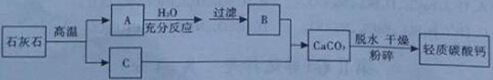
请分析轻质碳酸钙的生产流程,回答下列问题:
(1)物质B的化学式为 ;
(2)在A→B之间,过滤操作的目的是 ;
(3)在B+C→CaCO3的过程中,应控制物质C的流量,原因是 (用化学方程式表示);
(4)生产轻质碳酸钙的方法很多请再设计一种制备方法 (用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
工业上采用氨碱法生产纯碱(NaCO3),主要流程如图1:
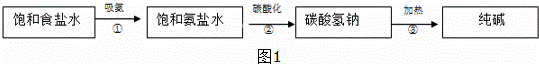
(1)在①〜③三个过程中,发生分解反应的是 (填序号).
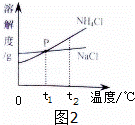
(2)我国化学家侯德榜在氨碱法的基础上创立的“侯氏制碱法“,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl. NH4Cl和NaCl的溶解度曲线如图2所示.
①写出一条P点表示的意义 .
②将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会 (填“变大”“变小”“不变”之一).
③当NH4Cl固体中含有少量NaCl时,可采用降温结晶的方法提纯NH4Cl,请说明提纯的原理: .
查看答案和解析>>
科目: 来源: 题型:
二十一世纪是海洋开发与利用的世纪,我市实施黄蓝两大国家战略形成新的发展格局,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水晒盐:将海水引入蒸发池,经日晒蒸发到一定程度时,导入结晶池,继续日晒,海水就会成为食盐的饱和溶液,再晒就会逐渐析出粗盐,剩余的液体称为母液(也称卤水)。
1L海水在逐渐浓缩过程中不断析出的盐的种类和质量(单位:g)关系如下表所示:
| 海水密度(g/mL) | CaSO4 | NaCl | MgCl2 | MgSO4 |
| 1.20 | 0.91 | |||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 |
| 1.31 | 1.40 | 0.54 | 0.03 |
I、海水晒盐是 (选填“物理”或“化学”)变化,包含蒸发、 等过程。
II、若得到纯度较高的粗盐和含浓度较高的卤水,卤水的密度应控制在什么范围 。
(2)海水制镁:海水晒盐后,以其母液(卤水)和贝壳(主要成分是CaCO3)为原料制镁,其工艺流程如下图所示:
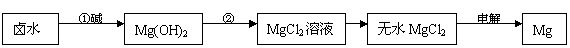

I、步骤①所加的碱应该是 (选填“氢氧化钠”或“石灰乳”),步骤②反应的化学方程式是 ;若要验证镁、铁、铜的活动性顺序,选择铁丝后,还要选择 、 两种溶液。
II、Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物,某些阻燃剂(阻碍燃烧的物质)的有效成分是Mg(OH)2。你认为Mg(OH)2能够阻燃的原因可能是 (选填序号)
A、Mg(OH)2分解需要吸收大量的热,降低了可燃物的着火点
B、生成的氧化镁覆盖在可燃物表面,隔绝了空气
C、生成的水蒸气降低了可燃物周围氧气浓度
D、反应因吸热降低了环境温度,使可燃物不易达到着火点
查看答案和解析>>
科目: 来源: 题型:
海洋中蕴含丰富的资源.
(1)海水淡化是解决淡水资源不足的重要方法.下列方法中,可以使海水变为淡水的是 (填字母序号).
A.滤纸过滤 B.吸附 C.沉降 D.蒸馏
(2)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和热传热介质.重水中重氢原子(D)的相对原子质量是2,则重水中氢元素的质量分数为 .
(3)从海水中制备纯碱和金属镁的流程如图所示:
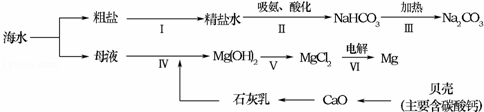
回答下列问题:
①步骤Ⅴ中所加试剂是 .
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下了物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为 (填字序号).
a.适量的盐酸 b.稍过量的Na2CO3溶液 c.稍过量的Ba(OH)2溶液
③第Ⅲ歩反应的化学方程式是 .
④在海边用贝壳作原料制生石灰,比用石灰石作原料的优点是 (写一条).
查看答案和解析>>
科目: 来源: 题型:
浩瀚的大海里蕴藏着丰富的资源,开发海水资源前景广阔,探究学习小组以含有Ca2+,Mg2+,Cl﹣离子的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2,流程如图1:
请回答下列问题:

(1)操作Ⅰ中用到的玻璃仪器有烧杯、玻璃棒、 .
(2)以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式 .
(3)操作Ⅱ酸化时应选择的酸是 (填写化学式).
(4)上述反应中未涉及的基本反应类型是 (填写字母标号)
a.复分解反应 b.置换反应 c.化合反应 d.分解反应
(5)回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成CH4和O2,该反应的化学方程式为 ,紫外线照射时,在不同催化剂(①、②、③)的作用下,CH4产量随光照时间的变化如图2所示,在第10小时时CH4产量最高是 (填写“①”、“②”、或“③”).
(6)已知T℃时四种化合物在水中和液氨中的溶解度如下表:
| AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
| H2O(1) | 170g | 92.0g | 1.50×10﹣4g | 33.3g |
| NH3(1) | 86.0g | 97.2g | 0.80g | 0.00g |
上述四种物质能在液氨中发生复分解反应的化学方程式为
.
查看答案和解析>>
科目: 来源: 题型:
金属(Ti)具有熔点高、密度小、抗腐蚀,易于加工等优良性能,被誉为“未来的金属”。工业上以钛酸铁(FeTiO3)等原料经过一系列反应制备纳米二氧化钛和钛。主要生产过程如下:(其他产物已略去)
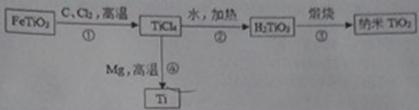
⑴反应①生成两种氧化物和一种有毒的氧化物气体,该气体的化学是 。
⑵反应②的化学方程式是 。
⑶纳米二氧化钛中钛元素的化合价为 价。
⑷反应①②③④中属于置换反应的是 (填序号)。
查看答案和解析>>
科目: 来源: 题型:
济宁是山东省重要的煤炭能源基地,然而矿区废水中Fe2+、Cu2+、Zn2+等严重影响着当地水质。某污水处理厂采用下图工艺(见下图)净化这种酸性废水并回收Fe2+、Cu2+、Zn2+三种离子。请读识流程图并回答:

(1)矿区废水经氧化池后再进入沉淀池Ⅰ,目的是_______________________________;
(2)利用氢氧化钠调节沉淀池Ⅰ、沉淀池Ⅱ和沉淀池Ⅲ的pH,目的是_________________;
(3)出水前,中和池中加入硫酸的作用___________________;
(4)若矿区废水中主要含有硫酸盐,请写出沉淀池Ⅲ中发生反应的化学方程式_________。
查看答案和解析>>
科目: 来源: 题型:
工业用煤燃烧产生二氧化硫,在排放前需经处理,如图是两种除硫工艺中主要物质的转化路径(部分产物已略).若每1000g Ca(OH)2和NaOH的市场价格分别按0.36元、2.90元计算,下列说法不正确的是()
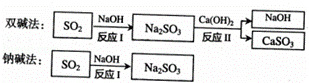
A. 煤是不能再生的化石燃料
B. 反应Ⅰ的化学反应方程式为:SO2+2NaOH=Na2SO3+H2O
C. “双碱法”中的NaOH可以循环使用,节约成本
D. 处理相同的SO2,“钠碱法”所需的原料成本更低
查看答案和解析>>
科目: 来源: 题型:
示例:硫在空气、氧气中燃烧,化学反应相同,但反应现象不同.说明反应物的浓度不同,反应现象不同.请参照示例回答下列问题:
(1)碳在氧气不足、氧气充足的条件下燃烧,反应物相同,但产物不同.说明 不同,产物不同.
(2)二氧化碳与水反应,在常温下生成碳酸,在叶绿体、光照的条件下发生光合作用生成葡萄糖和氧气.反应物相同,但产物不同.说明 不同,产物不同.
(3)细铁丝(或铁粉)在氧气中能剧烈燃烧,铁钉(或铁制燃烧匙)在氧气中不能燃烧,反应物相同,但反应的速率不同.说明反应物的 不同,反应的速率不同.
查看答案和解析>>
科目: 来源: 题型:
实验小组同学做了如下实验。


(1)A中反应的化学方程式为 ,将带火星的木条置于a处,若观察到 ,说明已有氧气产生。
(2)B中现象是声带涌出柱状的泡沫,可形象地称为“大象牙膏”,其原理主要是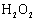 在某些催化剂作用下迅速分解产生水和氧气。反应的化学方程式为 。
在某些催化剂作用下迅速分解产生水和氧气。反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com