
科目: 来源: 题型:解答题
 兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表:
兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表:| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
查看答案和解析>>
科目: 来源: 题型:解答题
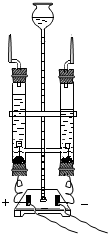
 如图是实验室电解水的简易装置示图,则
如图是实验室电解水的简易装置示图,则查看答案和解析>>
科目: 来源: 题型:选择题
| A. | KMnO4═K2MnO4+MnO2+O2↑ | B. | CaCO3+2HCl═CaCl2+CO2↑+H2O | ||
| C. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO | D. | 2Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$Fe2O3 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在装有过氧化氢溶液的试管中将带火星的木条伸入试管中 | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢 |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 产生大量气泡 带火星的木条复燃 | 加入Al2O3后过氧化氢溶液分解速率变快 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
 小明同学用稀盐酸与碳酸钙反应证明“质量守恒定律”,设计的实验装罝如图所示.
小明同学用稀盐酸与碳酸钙反应证明“质量守恒定律”,设计的实验装罝如图所示.查看答案和解析>>
科目: 来源: 题型:解答题
 水是生命之源.
水是生命之源.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com