
科目: 来源: 题型:解答题
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 所取合金的质量∕g | 10 | 10 | 20 | 30 |
| 所加稀硫酸的质量∕g | 100 | 120 | 80 | X |
| 生成氢气的质量∕g | 0.3 | 0.3 | 0.3 | Y |

| 实验序号 | 铁的氧化物质量/g | 生成铁的质量/g |
| 1 | 4.00 | 2.81 |
| 2 | 8.00 | 7.62 |
| 3 | 10.00 | 7.01 |
| 4 | 12.00 | 8.42 |
| 5 | 14.00 | 9.81 |
| 6 | 16.00 | 11.22 |
| 7 | 18.00 | 12.63 |
| 8 | 20.00 | 14.03 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向滤渣中加入稀盐酸,可能有气泡产生 | |
| B. | 滤渣中一定含有Ag和Cu | |
| C. | 滤液中一定含有Cu(NO3)2和Al(NO3)3,可能含有AgNO3 | |
| D. | 滤液中一定含有Cu(NO3)2,一定不含AgNO3,可能含有Al(NO3)3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将光亮的铜丝插入稀盐酸中,有气泡产生 | |
| B. | 镁条在空气中燃烧时,发出耀眼的白光 | |
| C. | 木炭在氧气中燃烧呈红热状态 | |
| D. | 用6B铅笔代替石墨做导电性实验灯泡不亮 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 减少化石燃料的使用,多开发利用太阳能、风能、地热能等 | |
| B. | 减少使用私家车次数,多乘公交车或骑自行车,实现“低碳生活” | |
| C. | 尽量多使用一次性餐具,既方便又卫生 | |
| D. | 废旧电池不随意丢弃,可回收利用以便节约金属资源并减少污染 |
查看答案和解析>>
科目: 来源: 题型:解答题
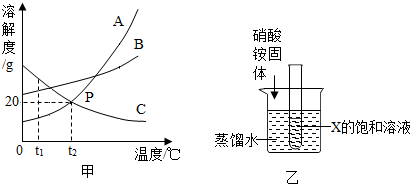
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
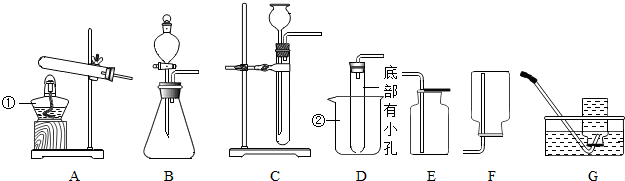
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com