
科目: 来源: 题型:选择题
| A. | 明矾溶液可以区分硬水和软水 | |
| B. | 自来水厂净化水的过程,发生的变化都是物理变化 | |
| C. | 为了节约用水,可以用工业废水直接浇灌农田 | |
| D. | 水与过氧化氢的组成元素相同,均可通过化学反应生成氧气 |
查看答案和解析>>
科目: 来源: 题型:解答题
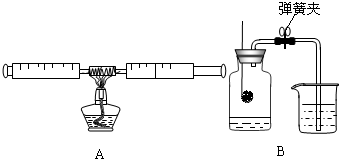 小红用如图所示的A装置测定空气中氧气的含量.硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有30mL室温下的空气.回答下列问题:
小红用如图所示的A装置测定空气中氧气的含量.硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有30mL室温下的空气.回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
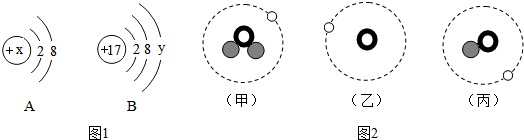
 道耳顿模型特点:不可再分的实心球体
道耳顿模型特点:不可再分的实心球体  汤姆生模型特点:正负电荷均匀分布
汤姆生模型特点:正负电荷均匀分布 卢瑟福模型特点:核位于原子中心,质量集中在核上.
卢瑟福模型特点:核位于原子中心,质量集中在核上. ”表示质子,“
”表示质子,“ ”表示中子,“○”表示电子.请通过比较归纳:
”表示中子,“○”表示电子.请通过比较归纳:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com