
科目: 来源: 题型:选择题
| 资料:甲的溶解度 | |||||
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
| A. | ①和②中甲的质量分数相等 | B. | ②和③中都有固体存在 | ||
| C. | ③和⑤的溶液都是饱和溶液 | D. | ④和⑤中没有固体存在 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 待鉴别物质 | 方法和所加试剂 | |
| 方法一 | 方法二 | ||
| A | 稀HCl和稀H2SO4 | 滴加BaCl2溶液 | 加入酚酞试液 |
| B | CaCO3和BaSO4 | 滴加稀HCl | 加入足量水 |
| C | 稀HNO3和KOH溶液 | 用pH试纸检验 | 滴加CuSO4溶液 |
| D | Ca(OH)2溶液和NaOH溶液 | 滴加K2CO3溶液 | 滴加FeCl3溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| X | Y | Z | W | |
| 盐酸 | √ | ─ | ─ | √ |
| Z的硝酸盐 | √ | |||
| W的硝酸盐 | √ | ─ |
| A. | X>Y>W>Z | B. | W>X>Y>Z | C. | X>W>Y>Z | D. | Y>W>Z>X |
查看答案和解析>>
科目: 来源: 题型:解答题
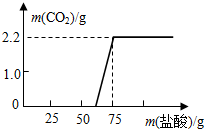 实验室中久置的NaOH会因为吸收空气中的CO2而变质.为了测定实验室中久置的NaOH的变质程度,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,确定样品中NaOH的变质程度.若实验测得加入稀盐酸的质量与产生的CO2气体的质量关系如图所示.请根据图象分析计算:
实验室中久置的NaOH会因为吸收空气中的CO2而变质.为了测定实验室中久置的NaOH的变质程度,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,确定样品中NaOH的变质程度.若实验测得加入稀盐酸的质量与产生的CO2气体的质量关系如图所示.请根据图象分析计算:查看答案和解析>>
科目: 来源: 题型:解答题
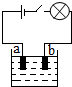 某同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如下表:
某同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如下表:| 物质 导电性 状态 | 食盐NaCl | 硝酸钾KNO3 | 蔗糖C12H22O11 | 氢氧化钠NaOH | 硫酸铜CuSO4 |
| 固态 | × | × | × | × | × |
| 熔化状态 | √ | √ | × | √ | √ |
| 水溶液 | √ | √ | × | √ | √ |
查看答案和解析>>
科目: 来源: 题型:解答题
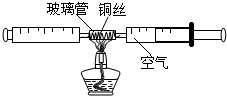 在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,直至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.
在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,直至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.查看答案和解析>>
科目: 来源: 题型:解答题
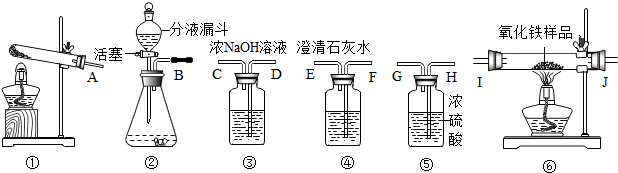
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶质的溶解度变小 | B. | 单位体积内的OH-数目不变 | ||
| C. | 溶质的质量分数变大 | D. | 溶液中溶质质量不变 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 第一次 | 第二次 | 第三次 | |
| O2的质量(g) | 1.5 | 2 | 3 |
| SO2的质量(g) | 3 |
查看答案和解析>>
科目: 来源: 题型:解答题
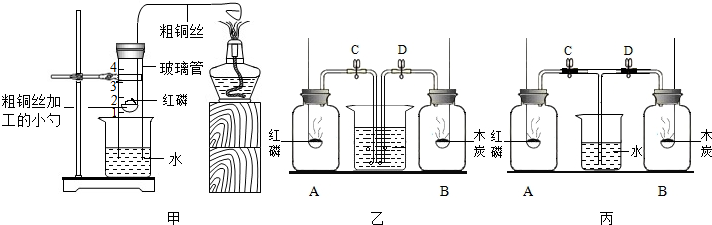
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com