
科目: 来源: 题型:选择题
| A. | 滴加CaCl2溶液 | B. | 滴加稀盐酸 | C. | 滴加Ca(OH)2溶液 | D. | 滴加石蕊试液 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| SO2最高质量分数限值(单位:mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
查看答案和解析>>
科目: 来源: 题型:解答题
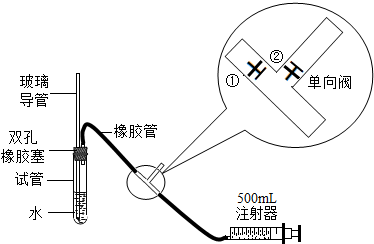
 菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:
菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 邻苯二甲酸二辛酯是氧化物 | |
| B. | 邻苯二甲酸二辛酯中碳元素质量分数最高 | |
| C. | 邻苯二甲酸二辛酯中碳、氧元素质量比为6:1 | |
| D. | 邻苯二甲酸二辛酯中有24个碳原子,38个氢原子,4个氧原子 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com