
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
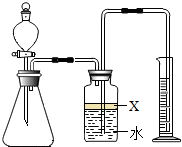 氮化铝(AlN)是一种新型材料.某氮化铝样品中含有碳或氧化铝杂质.已知氮化铝和NaOH溶液能反应,其反应方程式为:
氮化铝(AlN)是一种新型材料.某氮化铝样品中含有碳或氧化铝杂质.已知氮化铝和NaOH溶液能反应,其反应方程式为:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 | |
| 步骤l | 取少量干燥的孔雀石样品置于大试管中进行加热 | (1)残留固体呈黑色 (2)大试管内壁有水珠 | 孔雀石加热分解的产物有水. |
步骤2 | 完全加热后在试管中加入足量稀硫酸 | (3)黑色固体完全溶解,溶液变成蓝色 | 黑色的固体只有CuO没有C |
查看答案和解析>>
科目: 来源: 题型:选择题
 2011年3月15日,日本地震及海啸灾难第五天,各国救援队正深入岩手县等灾区搜救生命,生还者向救援队鞠躬致意.救援人员为搜索埋在废墟下的幸存者,用了许多搜救犬.搜救犬能根据人体发出的气味发现幸存者.从微观的角度分析搜救犬能发现幸存者的原因是( )
2011年3月15日,日本地震及海啸灾难第五天,各国救援队正深入岩手县等灾区搜救生命,生还者向救援队鞠躬致意.救援人员为搜索埋在废墟下的幸存者,用了许多搜救犬.搜救犬能根据人体发出的气味发现幸存者.从微观的角度分析搜救犬能发现幸存者的原因是( )| A. | 分子的质量很小 | B. | 分子的不断运动 | ||
| C. | 不同分子性质不同 | D. | 分子间有间隙 |
查看答案和解析>>
科目: 来源: 题型:解答题
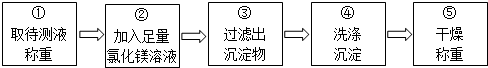
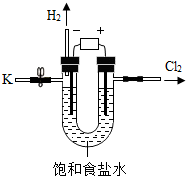 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com