
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
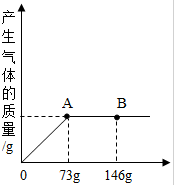 一烧杯中盛有30.8gBaCO3和BaCl2的粉末状混合物,向其中逐滴加入溶质的质量分数为10%的稀盐酸,产生气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答下列问题:
一烧杯中盛有30.8gBaCO3和BaCl2的粉末状混合物,向其中逐滴加入溶质的质量分数为10%的稀盐酸,产生气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
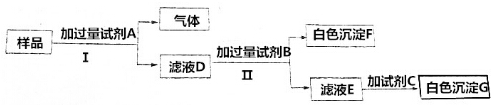
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
| 阴离子 阳离子 | OH- | Cl- | CO32- | HCO3- |
| H+ | 溶、挥 | 溶、挥 | 溶、挥 | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 溶 |
| 实验步骤 | 实验操作 | 实验中可能出现的现象 | 相应结论 |
| 一 | 向A的试样中加入足量的水 | ①AA的试样全部溶解 | A是 Na2CO3和NaHCO3 |
| ②A的试样部分溶解 | A是NaHCO3和CaCO3或Na2CO3和CaCO3 | ||
| 二 | 若A的试样部分溶解则向其滤液中加入酚酞试液 | ③溶液显红色 | A是Na2CO3和CaCO3 |
| ④溶液显浅红色 | A是NaHCO3和CaCO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
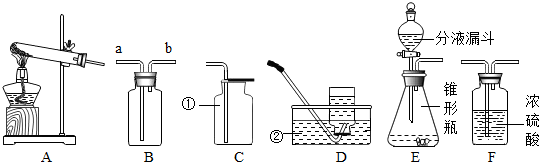
查看答案和解析>>
科目: 来源: 题型:解答题
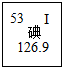 碘元素是人体必需的微量元素之一.
碘元素是人体必需的微量元素之一.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com