
科目: 来源: 题型:选择题
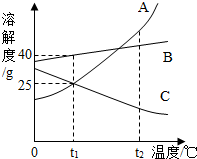
| A. | t2℃时,三种物质的饱和溶液中A溶液的溶质质量分数最大 | |
| B. | t1℃时,三种物质的溶解度由大到小的顺序为:B>A=C | |
| C. | 要将C的接近饱和的溶液转化为饱和溶液可以采用升温的方法 | |
| D. | A中混有少量B,可采用冷却热饱和溶液的方法提纯A |
查看答案和解析>>
科目: 来源: 题型:多选题
| 事实 | 解释 | |
| A | 氖气和氦气化学性质相似 | 氖原子和氦原子最外层电子数相同 |
| B | 氯化钠固体不导电 | 因为没有带电的离子 |
| C | 空气比水容易被压缩 | 混合物比纯净物分子间隔大 |
| D | 物质的热胀冷缩 | 粒子间的间隔随温度的改变而改变 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | FeSO4 | B. | FeSO4、ZnSO4 | C. | Fe2(S04)3、ZnS04 | D. | FeSO4、CuSO4 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论或有关化学反应方程式 |
| 取样,溶解,滴加少量稀盐酸 | 产生气泡 | 该化肥是K2CO3 方程式:K2CO3+2HCl═2KCl+H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:解答题
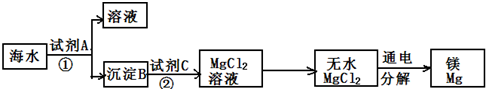
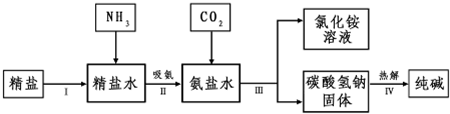
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生白色沉淀 | 反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想②成立 |
查看答案和解析>>
科目: 来源: 题型:解答题
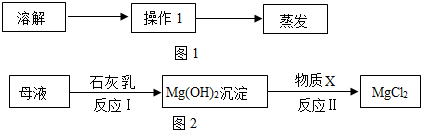
查看答案和解析>>
科目: 来源: 题型:解答题
 通过化学学习,我们认识了酸、碱、盐的化学性质,请用所学知识回答下列两小题:
通过化学学习,我们认识了酸、碱、盐的化学性质,请用所学知识回答下列两小题:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com