
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取“石灰”样品于试管中,加入适量水,振荡充分反应后,取上层清液并向其中加入几滴酚酞试液 ②取“石灰”样品与水反应后的不溶物于试管中,加入足量的稀盐酸 | ①酚酞试液变红 ②有气泡产生 | 猜想Ⅲ成立 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:推断题
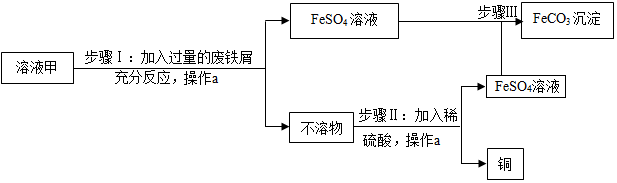
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:推断题
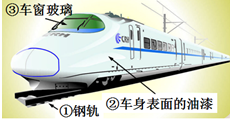 高速铁路可以加快出行步伐.2015年12月6日,南京至安庆高铁将正式开通运营,使苏、皖、赣、鄂四省连为一体.结合所学化学知识,回答下列问题:
高速铁路可以加快出行步伐.2015年12月6日,南京至安庆高铁将正式开通运营,使苏、皖、赣、鄂四省连为一体.结合所学化学知识,回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化合物是含有不同元素的纯净物,则含有不同种元素的纯净物一定是化合物 | |
| B. | 铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用 | |
| C. | 浓硫酸具有吸水性,则浓盐酸也具有吸水性 | |
| D. | 分子、原子可以构成物质,则物质一定都是由分子、原子构成的 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 洗涤剂能去除衣服上的油污 | 洗涤剂具有乳化作用 |
| B | 二氧化碳能使紫色石蕊试液变红 | 二氧化碳具有酸性 |
| C | 温度计中的水银能指示温度 | 汞原子间距离随温度升高而增大 |
| D | 打开汽水瓶盖时,汽水会自动喷出 | 气体的溶解度随压强减小而减小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:填空题
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水蒸气 | W |
| 反应前质量/g | 48 | 80 | 0 | 0 | 0 |
| 反应后质量/g | 2 | 0 | 44 | 54 | x |
查看答案和解析>>
科目: 来源: 题型:解答题

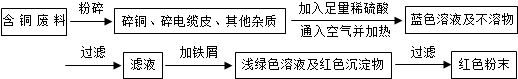
查看答案和解析>>
科目: 来源: 题型:解答题
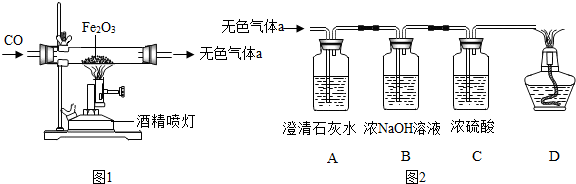
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com