
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 25 | 25 | 50 |
| 所用稀硫酸的质量/g | 120 | 160 | 100 |
| 生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
查看答案和解析>>
科目: 来源: 题型:解答题
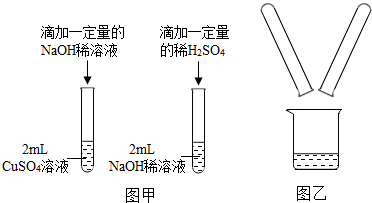 某化学兴趣小组在实验室做了如图甲所示的A、B两个实验.
某化学兴趣小组在实验室做了如图甲所示的A、B两个实验.| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴入 酚酞溶液 | 无色溶液变红色 | 假设4正确 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 欲测定某生石灰中碳酸钙的质量分数,进行了如图实验.请计算:
欲测定某生石灰中碳酸钙的质量分数,进行了如图实验.请计算:查看答案和解析>>
科目: 来源: 题型:解答题
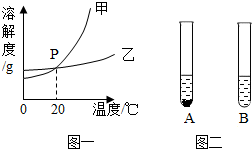 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应后所得的气体是纯净物 | |
| B. | 反应后气体与原混合气体的物质的量之比为3:4 | |
| C. | 参加反应的CO和O2的物质的量之比为3:2 | |
| D. | 反应后的气体中C、O原子的物质的量之比为3:7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com