
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加AgNO3溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
查看答案和解析>>
科目: 来源: 题型:填空题
| 猜想与假设 | 操作方法 | 证明猜想正确的实验现象 |
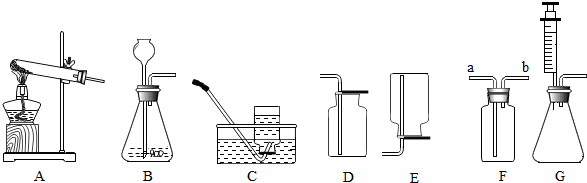
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 为了防止疾病传染,提必人们生活质量,尽量使用一次性餐具 | |
| B. | 不能长时间把“QQ”挂在线上,即用即上线 | |
| C. | 用传统发条式闹钟代替电子闹钟 | |
| D. | 减少使用私家车次数,多乘公交或骑自行车 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com