
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:填空题
| 定时间 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
查看答案和解析>>
科目: 来源: 题型:填空题
| 盐酸溶液 浓度 | 反应开始时酸溶液的 温度 | 反应开始到2分钟产生的 气体体积 | 反应结束共产生 气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 102mL | 175mL |
查看答案和解析>>
科目: 来源: 题型:填空题
| 实验 | 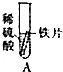 | 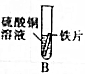 | 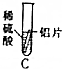 | 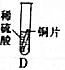 | 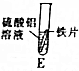 |
| 现象 | 有气泡产生,产生气泡较慢 | 铁片上有红色物质附着,溶液变成浅绿色 | 有气泡产生,产生气泡较快 | 无现象 | 无气泡产生无明显现象 |
查看答案和解析>>
科目: 来源: 题型:填空题
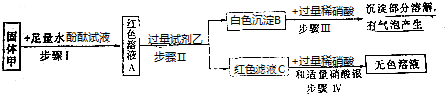
查看答案和解析>>
科目: 来源: 题型:实验探究题
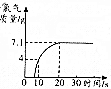 实验室用足量二氧化锰与浓盐酸加热制取氯气,当反应时氯化锰与氯化氢混合溶液中氯化氢的质量分数降低至20%,反应停止.反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.
实验室用足量二氧化锰与浓盐酸加热制取氯气,当反应时氯化锰与氯化氢混合溶液中氯化氢的质量分数降低至20%,反应停止.反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.查看答案和解析>>
科目: 来源: 题型:填空题
 如图是A、B、C三种固体物质的溶解度曲线,据图回答问题:
如图是A、B、C三种固体物质的溶解度曲线,据图回答问题:查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 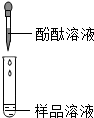 | 若溶液变红,猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是碳酸钠也可以使酚酞变成红色 |
| 第2组 | 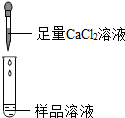 | 若产生白色沉淀,则猜想一不成立. | 第3组同学认为:此方案能确定有Na2CO3(填化学式)存在. |
| 第3组 | 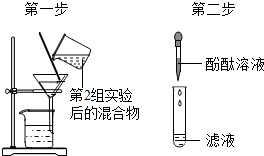 | 若滤液不变红,则猜想二成立;若滤液变红,则猜想三成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是将第二组实验沉淀之后取滤液. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com