
科目: 来源: 题型:选择题
| A. | 焚烧塑料是减少白色污染的有效方法 | |
| B. | 目前氢能源没有广泛推广的主要原因是淡水资源缺乏 | |
| C. | 空气中CO2含量超标会引起温室效应 | |
| D. | 化工厂可利用通过加高烟囱排放废气,防止形成酸雨 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D |
 |  | 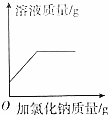 | 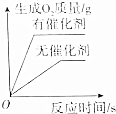 |
| 电解水 | 向pH=2的稀盐酸中加入pH=12的氢氧化钠溶液 | 20℃时,向一定量氯化钠饱和溶液中加入氯化钠固体 | 用等质量氯酸钾分别制取氧气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
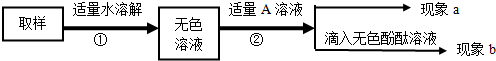
| 第一步: 用试管取约2mL该溶液,滴入适量氢氧化钙溶液,振荡. | 现象a:白色沉淀 | 化学方程式: ①Na2CO3+Ca(OH)2=2NaOH+CaCO3↓,有碳酸钠并全部除尽. |
| 第二步: 静置,取上层清液于试管中滴入酚酞溶液,振荡. | 现象b: ②液体变红 | 含有NaOH,猜想三成立,是NaOH和Na2CO3混合物 |
| 实验操作 | 实验现象 | 实验结论 |
查看答案和解析>>
科目: 来源: 题型:解答题
 用于治疗流感的抗病毒药物“达菲”可以有效地预防和治疗甲型H1N1流感.从烹调香料八角中提取到的莽草酸是制取“达菲”的主要原料,如图是莽草酸的一些基本性质.请回答:
用于治疗流感的抗病毒药物“达菲”可以有效地预防和治疗甲型H1N1流感.从烹调香料八角中提取到的莽草酸是制取“达菲”的主要原料,如图是莽草酸的一些基本性质.请回答:查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:解答题
 如图是小鹏同学设计的对比实验,用于证明二氧化碳和氢氧化钠能否反应.小燕同学认为该实验设计不符合对比实验的基本原则,她的理由是什么?写出塑料瓶中发生反应的化学方程式.
如图是小鹏同学设计的对比实验,用于证明二氧化碳和氢氧化钠能否反应.小燕同学认为该实验设计不符合对比实验的基本原则,她的理由是什么?写出塑料瓶中发生反应的化学方程式.查看答案和解析>>
科目: 来源: 题型:填空题
 A、B、C、D是四种含有相同金属元素的白色固体,它们的转化关系如右图所示(部分物质已略去).其中A的相对分子质量为100,C是常见的干燥剂,D是配制农药波尔多液的试剂.
A、B、C、D是四种含有相同金属元素的白色固体,它们的转化关系如右图所示(部分物质已略去).其中A的相对分子质量为100,C是常见的干燥剂,D是配制农药波尔多液的试剂.查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验序号 | A | B | C | D |
| 试剂 | 蒸馏水 | 稀盐酸 | NaOH溶液 | NaCl溶液 |
| 电流强度/mA | 约为0 | 0.09 | 0.09 | 0.09 |
查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com