
科目: 来源: 题型:解答题
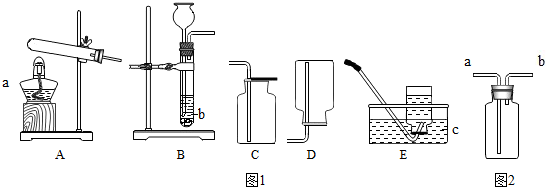
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 随着人们生活水平的提高,汽车已经走进了千家万户,成为许多家庭的代步工具.也许你的家庭就拥有一台不错得轿车,那就请根据你对汽车的了解及所学的化学知识回答下列问题:
随着人们生活水平的提高,汽车已经走进了千家万户,成为许多家庭的代步工具.也许你的家庭就拥有一台不错得轿车,那就请根据你对汽车的了解及所学的化学知识回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用氢氧化钠溶液吸收二氧化碳:CO2+2NaOH═Na2CO3+H2O 复分解反应 | |
| B. | 溶洞的形成:CaCO3+H2O+CO2═Ca(HCO2)2 化合反应 | |
| C. | 实验室制取氢气:Fe+2HCl═FeCl2+H2 置换反应 | |
| D. | 用氢氧化镁治疗胃酸过多:Mg(OH)2+H2SO4═MgSO4+2H2O 中和反应 |
查看答案和解析>>
科目: 来源: 题型:多选题
 维生素(C6H8O6)是人体必需的重要营养素之一,维生素C对提高自身免疫力有很大帮助.下列关于维生素C(简称Vc)的说法中,正确的是( )
维生素(C6H8O6)是人体必需的重要营养素之一,维生素C对提高自身免疫力有很大帮助.下列关于维生素C(简称Vc)的说法中,正确的是( )| A. | Vc分子中含20个原子核 | |
| B. | Vc是由碳、氢、氧三种原子构成的 | |
| C. | Vc分子中碳、氢、氧元素的质量比是9:l:l2 | |
| D. | Vc分子中质子数与电子数之比为l:1 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
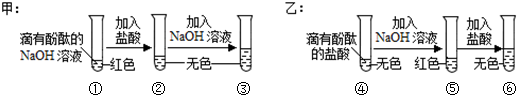
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com