
科目: 来源: 题型:选择题
| A. |  Ca(OH)2的溶解度曲线 | |
| B. |  往一定量Ba(OH)2溶液中加入稀硫酸 | |
| C. |  等质量Mg和Zn 加入足量盐酸 | |
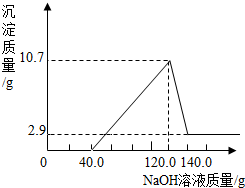
| D. | 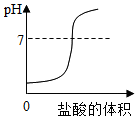 往一定量的氢氧化钠溶液中加入稀盐酸 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
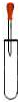 在实验课上,老师让同学们分组实验探究,自己设计实验证明氢氧化钠与盐酸恰好完全反应.下面是来自不同小组的三位同学的实验过程,请你帮他们分析解决实验中遇到的问题.
在实验课上,老师让同学们分组实验探究,自己设计实验证明氢氧化钠与盐酸恰好完全反应.下面是来自不同小组的三位同学的实验过程,请你帮他们分析解决实验中遇到的问题.查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:选择题
| A.除杂的方法 | B.物质与俗名 |
| ①粗盐难溶性杂质去除--溶解、过滤、蒸发、干燥 ②木炭粉中混有铁粉--用磁铁吸引 ③CaO中混有石灰石--高温煅烧 | ①乙醇--酒精 ②碳酸钠--纯碱、苏打 ③氢氧化钠--火碱、烧碱、苛性钠 |
| C.安全常识 | D.化学与生活 |
| ①厨房煤气管漏气--关闭阀门并开窗通风 ②实验时碰倒酒精灯着火--用湿抹布盖灭 ③冬天用煤炉取暖--保证室内通风 | ①人体缺铁会引起贫血症 ②多吃水果蔬菜利于补充维生素 ③使用可降解塑料可减少“白色污染” |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:选择题
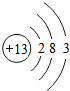 ;④SO3.
;④SO3.| A. | ①中的数字“3”表示三个氢原子 | |
| B. | ②中的数字“3”表示铁元素的化合价为+3价 | |
| C. | ③中的数字“3”表示铝原子有三个电子层 | |
| D. | ④中的数字“3”表示一个SO3分子中含有一个 O3分子. |
查看答案和解析>>
科目: 来源: 题型:解答题
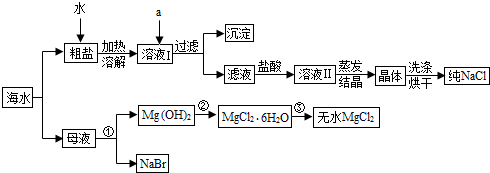
查看答案和解析>>
科目: 来源: 题型:解答题
 汽车制造是盐城市的支柱经济产业之一,汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空.(1)汽车制造中用得最多的金属材料是钢.钢不是(填“是”或“不是”)纯金属.车体表面喷漆不仅美观,而且可有效防止钢铁与水和氧气接触而生锈.炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
汽车制造是盐城市的支柱经济产业之一,汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空.(1)汽车制造中用得最多的金属材料是钢.钢不是(填“是”或“不是”)纯金属.车体表面喷漆不仅美观,而且可有效防止钢铁与水和氧气接触而生锈.炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com