
科目: 来源: 题型:选择题
| A. | 钠在氯气中燃烧时,钠原子得到电子 | |
| B. | 反应物钠由分子构成,生成物氯化钠由离子构成 | |
| C. | 钠能在氯气中燃烧,说明燃烧不一定需要氧气参与 | |
| D. | 钠在氯气中燃烧生成的氯化钠与家庭中食用的氯化钠化学性质不同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应物锂是金属单质 | B. | 该反应中MnO2是催化剂 | ||
| C. | Li2O2中氧元素的化合价显-2价 | D. | 该反应是化合反应 |
查看答案和解析>>
科目: 来源: 题型:实验探究题

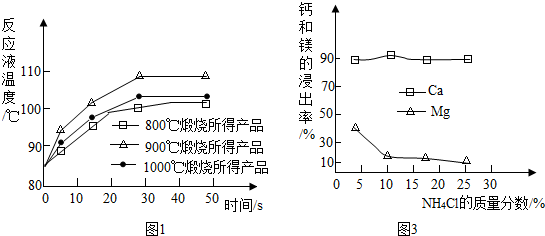
查看答案和解析>>
科目: 来源: 题型:实验探究题
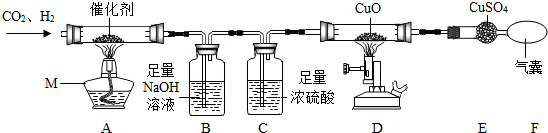
查看答案和解析>>
科目: 来源: 题型:填空题
| 项目 | 摄入量 | 推荐摄入量 |
| 蛋白质(g) | 72.9 | 65 |
| 脂肪(g) | 65.1 | 48.2~72.3 |
| 维生素C(mg) | 176 | 100 |
| 钙(mg) | 807 | 800 |
| 铁(mg) | 21 | 20 |
| 硒(mg) | 0.037 | 0.05 |
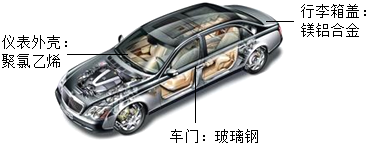
查看答案和解析>>
科目: 来源: 题型:多选题
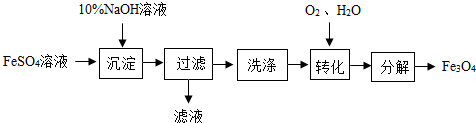
| A. | 理论上与FeSO4反应的NaOH溶液的质量为4.8t | |
| B. | 理论上“转化”过程参与反应的O2的质量为320kg | |
| C. | 该方法理论上最终可以获得Fe3O4的质量为4.64t | |
| D. | 若“转化”过程参与反应的O2过量,则最终所得固体的质量偏小 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 10 | 8 |
| 2 | 10 | 6 |
| 3 | 10 | 4 |
| 4 | 10 | 2 |
| 5 | 10 | 2 |
查看答案和解析>>
科目: 来源: 题型:选择题
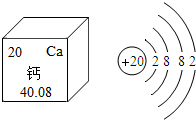 如图是钙元素在元素周期表中的信息及钙原子的原子结构示意图,下列关于钙元素的说法错误的是( )
如图是钙元素在元素周期表中的信息及钙原子的原子结构示意图,下列关于钙元素的说法错误的是( )| A. | 核内有20个质子 | |
| B. | 相对原子质量是40.08 | |
| C. | 属于非金属元素 | |
| D. | 在化学反应中,钙原子易失去两个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com