
科目: 来源: 题型:解答题

| 猜想 | 操作 | 现象 | 结论 |
假设:焰心 气体含石 蜡蒸气 | 取较长细玻璃管,用冷毛巾包住中部,将玻璃管下端插入焰心,上端使用火焰点燃 | 无火焰产生. | 假设成立 |
取下长玻璃管,打开湿毛巾 | 玻璃管内壁有一层石蜡颗粒. |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 诗句中涉及了化学变化 | |
| B. | 诗句中的“丝”含有的物质是维生素 | |
| C. | 诗句中的“灰”指的是蜡烛燃烧产生的CO2等气体和炭粒 | |
| D. | 诗句中的“泪”指的是液态石蜡 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | M的金属活动性比Ag强 | B. | 反应后溶液的质量增加 | ||
| C. | 金属M不可能变换成铝 | D. | 固体物质的质量增加了 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②③ | B. | ③⑤ | C. | ②⑤ | D. | ①④ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
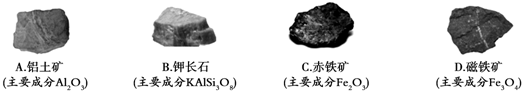
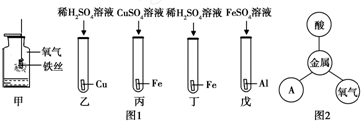

查看答案和解析>>
科目: 来源: 题型:实验探究题
 某化学兴趣小组在探究Mg、Fe、Cu的性质时进行了如图所示实验.
某化学兴趣小组在探究Mg、Fe、Cu的性质时进行了如图所示实验.| 操 作 | 现 象 | 结 论 |
| 取少量滤渣于试管中, 滴加稀盐酸 | 无明显现象 | 滤渣为Cu |
| 产生气泡,溶液变为浅绿色 | 滤渣为Cu和Fe |
查看答案和解析>>
科目: 来源: 题型:解答题
 某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);
某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com