
科目: 来源: 题型:实验探究题
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
| 试管编号 | 实验操作 | 实验现象 |
| 1号 | 0.5gCu(OH)2固体加入6mL0.6%的NaOH溶液 | 蓝色固体不消失 |
| 2号 | 0.5gCu(OH)2固体加入6mL1.0%的NaOH溶液 | 蓝色固体不消失 |
| 3号 | 0.5gCu(OH)2固体加入6mL20%的NaOH溶液 | 蓝色固体减少 |
| 4号 | 0.5gCu(OH)2固体加入6mL30%的NaOH溶液 | 蓝色固体消失,得到亮蓝色溶液 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:用洁净干燥的玻璃棒蘸取溶液,粘在pH试纸上,与标准比色卡对照 | 试纸变色,溶液pH<7 | 溶液中有HCl |
| 步骤2:取少量反应后溶液于试管中,滴加碳酸钠溶液振荡 | 先产生气泡,后产生沉淀 | 溶液中有CaCl2 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
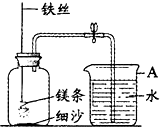 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1-6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7-9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色 |
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中, 充分振荡 | 沉淀不消失 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀消失,溶液变成亮蓝色 | 猜想二正确 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 探究过程 | K2CO3) | (NH4)2SO4 | 结论及化学方程式 |
| (1)分别取碳酸钾和硫酸铵固体,加入足量水溶解,取溶液分别滴入紫色石蕊溶液,观察溶液颜色变化 | 变蓝 | 变红 | 碳酸钾溶液显碱性 硫酸铵溶液显酸性 |
| (2)另取两种溶液分别加入足量 稀盐酸,观察现象 | 产生气泡 | 无明显现象 | 产生气泡的化学方程式 2HCl+K2CO3=2=KCl+CO2↑+H2O |
| (3)再取两种溶液分别加入Ba(OH)2溶液,观察现象 | 产生白色沉淀 | 有白色沉淀生成,同时以刺激性气味气体产生 | (NH4)2SO4与Ba(OH)2反应方程式 NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com