
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
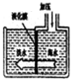 淡水海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水,以下分析中不正确的是( )
淡水海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水,以下分析中不正确的是( )| A. | 这种淡化膜不可用滤纸代替 | B. | 左侧池中的淡水属于软水 | ||
| C. | 右侧池中溶剂的质量不变 | D. | 右侧池中海水的溶质质量分数增大 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题

| A中浓硫酸浓度 | 实验现象 | A中生成 气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验Ⅰ | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验Ⅱ | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验Ⅲ | 20% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:填空题
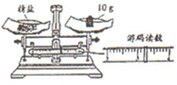 科学严谨的态度,安全规范的操作是成功进行化学实验的保障.
科学严谨的态度,安全规范的操作是成功进行化学实验的保障.查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
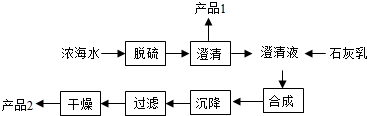
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
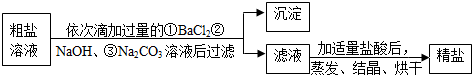
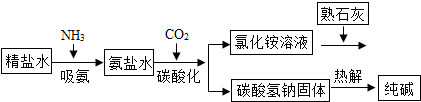
查看答案和解析>>
科目: 来源: 题型:推断题
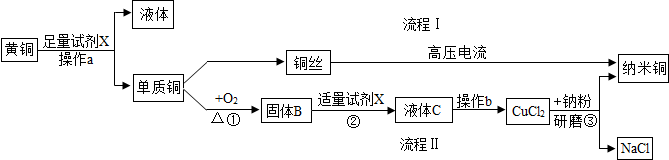
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com