
科目: 来源: 题型:选择题
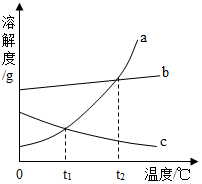 如图是a、b、c三种固体的溶解度曲线,下列说法不正确的是( )
如图是a、b、c三种固体的溶解度曲线,下列说法不正确的是( )| A. | t2℃时a、b的饱和溶液溶质质量分数相等 | |
| B. | 当b中含有少量a时,可以用蒸发结晶的方法提纯b | |
| C. | 通过降低温度可将c的饱和溶液变为不饱和溶液 | |
| D. | 将t2℃时a、b的饱和溶液降温至t1℃,析出晶体质量a一定大于b |
查看答案和解析>>
科目: 来源: 题型:实验探究题


查看答案和解析>>
科目: 来源: 题型:实验探究题
 同学们在实验室发现有一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分(如图)无法辨认具体是什么物质的溶液,只能看出溶质的质量分数为10%,经询问老师知道可能是氢氧化钠、氯化钠、氢氧化钙或碳酸钠溶液中的一种.为探究其成分,化学兴趣小组的同学进行如下探究,请你共同参与:
同学们在实验室发现有一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分(如图)无法辨认具体是什么物质的溶液,只能看出溶质的质量分数为10%,经询问老师知道可能是氢氧化钠、氯化钠、氢氧化钙或碳酸钠溶液中的一种.为探究其成分,化学兴趣小组的同学进行如下探究,请你共同参与:| 氢氧化钠 | 氯化钠 | 氢氧化钙 | 碳酸钠 | |
| 溶解度/g(20℃) | 51 | 36 | 0.16 | 21.5 |
| 实验操作及步骤 | 实验现象 | 实验结论 |
| 取少量样品溶液于试管中,滴加氯化钙溶液 | 有白色沉淀产生 | 该溶液是碳酸钠溶液 |
| 取少量样品溶液于试管中,滴加稀盐酸 | 有气泡产生 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:推断题
 物质A-D都是初中化学学过的物质,它们由如图所示的转化关系(反应条件已略),回答下列问题:
物质A-D都是初中化学学过的物质,它们由如图所示的转化关系(反应条件已略),回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com