
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:计算题
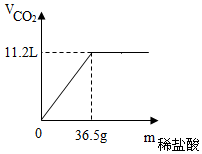 80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如图所示.试回答:
80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如图所示.试回答:查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 滤渣的质量一定大于a g,滤液的质量一定小于bg | |
| B. | 若滤渣中含有Fe,则滤液一定呈浅绿色 | |
| C. | 向滤渣中加入足量稀盐酸,滤渣全部溶解 | |
| D. | 若滤渣中只含有单质Cu,则滤液中至少含有两种金属阳离子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
| A. | 在20℃时,向100 g水中加入40 g硝酸钾固体,能够得到140 g溶液 | |
| B. | 随着溶液温度不断升高,硝酸钾固体的溶解度呈现出不断减少的趋势 | |
| C. | 60℃时210 g硝酸钾饱和溶液降温到20℃,能析出78.4 g硝酸钾晶体 | |
| D. | 在40℃时硝酸钾的饱和溶液中加入少量氯化钠固体,氯化钠不会溶解 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 煤矿的矿井要加强通风,防止发生爆炸 | |
| B. | 森林发生火灾,可用砍断树木形成隔离带 | |
| C. | 厨房天然气泄露,可打开抽油烟机排气 | |
| D. | 进入久未开启的地窖,要做灯火实验 |
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:选择题
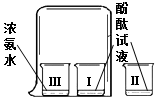
| A. | 氨水显碱性 | |
| B. | Ⅰ烧杯中酚酞变红,说明分子不断运动 | |
| C. | Ⅰ烧杯中酚酞试液变红,Ⅲ烧杯中浓氨水没有变色 | |
| D. | 温度越高,分子运动越快 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 医疗上用它来配制生理盐水 | |
| B. | 农业上用氯化钠选种 | |
| C. | 生活中用食盐来腌渍蔬菜、肉 | |
| D. | 常用晾晒海水的办法得到含较多杂质的粗盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com