
科目: 来源: 题型:选择题
| A. | 滤液中一定含有Zn2+,可能含有Cu2+ | |
| B. | 所得滤渣质量可能等于加入的Zn粉和Cu粉质量 | |
| C. | 如果滤渣中有Zn,则滤液可能为浅绿色 | |
| D. | 如果滤液中含有Ag+,则滤渣一定为纯净物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 焙制面包时加入适量碳酸氢钠 | B. | 用剧毒农药杀灭韭菜根部的害虫 | ||
| C. | 将亚硝酸钠当作食盐来食用 | D. | 用回收的食用油重复榨制食品 |
查看答案和解析>>
科目: 来源: 题型:解答题

| 固体M | 溶液N | 制取的气体 | 收集装置(填字母) |
| 大理石 | 稀盐酸 | CO2 | C |
| 锌粒 | 稀硫酸 | H2 | B或D |
| 二氧化锰 | 过氧化氢溶液 | O2 | B或C |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 方法 | 示例 |
| A | 实验法 | 用铜粉做“测定空气中氧气含量”的实验 |
| B | 分类法 | 根据组成物质的元素种类,将纯净物分为单质和化合物 |
| C | 归纳法 | 根据稀盐酸、稀硫酸等物质的化学性质,归纳出酸的通性 |
| D | 类推法 | 根据金属铝能与稀盐酸反应,推测金属铜也能与稀盐酸反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:实验探究题
 ”为铜片).
”为铜片).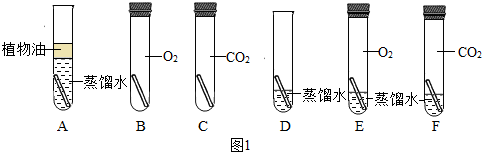
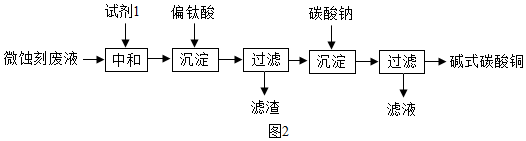
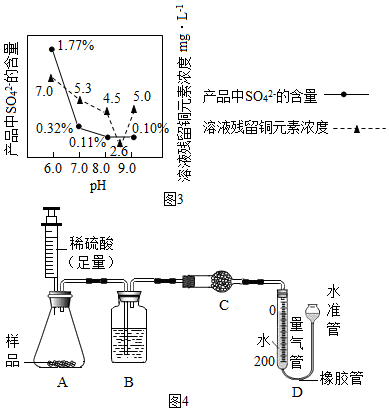
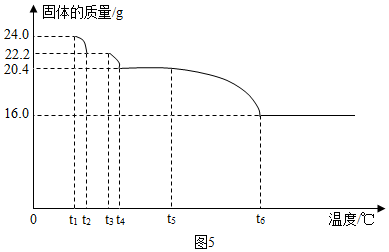
查看答案和解析>>
科目: 来源: 题型:填空题
 向硫酸铁溶液中投入一小块金属钠,反应剧烈,产生如图现象:
向硫酸铁溶液中投入一小块金属钠,反应剧烈,产生如图现象:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 通入CO质量大于8.4g | B. | 反应后剩余固体质量为6.8g | ||
| C. | 样品中氧化铁的质量分数为80% | D. | 上述反应过程中没有置换反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 熔点 | 密度 | 导电性 | 导热性 | 强度 | 抗腐蚀性 |
| 2500℃ | 3g/cm3 | 良好 | 良好 | 与钢相似 | 优异 |
查看答案和解析>>
科目: 来源: 题型:推断题
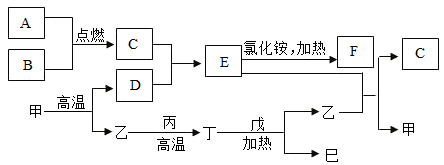
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com